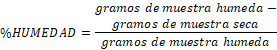1. Introducción
El Estero Salado es un estuario ubicado en el este de la ciudad de Guayaquil, desemboca en el golfo homónimo de la urbe, englobando en su recorrido alrededor de aproximadamente 93 km. Este brazo de mar; en conjunto con ciertas zonas bajas de los ríos Babahoyo y Daule constituyen un mismo ecosistema, al cual se le ha designado como Estuario Interior del Golfo de Guayaquil.
Desde que se planteó la problemática de contaminación por hidrocarburos del estuario del Estero Salado diferentes grupos de investigación han trabajado principalmente en los campos de medición de los niveles de contaminantes [1] y en los procesos de biodegradación in-situ y a escala de laboratorio [2].
Gracias a dichas investigaciones hoy conocemos que en el Sector Miraflores del estuario se encuentran los más altos niveles de hidrocarburos [1], además conocemos que entre los microorganismos endógenos del estuario existe una amplia variedad de Pseudomonas y de entre estos microorganismos existen algunas especies que pueden presentar capacidad para degradar hidrocarburos [2].
Existe una amplia diversidad en los métodos que se pueden emplear para este tipo de contaminación con hidrocarburos, que van desde ubicar los sedimentos en zonas consideradas seguras, pasando por la incineración de los residuos o tratamientos donde se aplican sustancias químicas u organismos vivos [3]. La Biorremediación, es uno de los mejores métodos para la limpieza de este tipo de residuos. Esencialmente por poseer costos de operación mucho más bajos, pero también porque ha sido utilizada de manera exitosa en contaminaciones de este tipo [4].
En algunas investigaciones se han separado cepas marinas degradadoras de hidrocarburos, de las cuales se ha enfatizado en la cepa Pseudomonas sp. F21, competente tanto para degradar hidrocarburos saturados lineales (TPH) como anillos aromáticos (HAP) propios de compuestos de crudo ligero [5].
Tiempo después se trabajó en analizar con mayor profundidad la capacidad de biodegradación microbiana de otros tipos de petróleo manipulando la cepa Pseudomonas sp. F21 [5].
La cantidad de variables que se pueden manipular para mejorar la eficiencia de los métodos de Biorremediación es amplia y se puede adaptar a las condiciones, en ocasiones se añaden nutrientes o se inocula de ciertos tipos de microorganismos el suelo (F6) [6]. De entre estas variables la que es primordial para todo tipo de remediación de hidrocarburos es la estructura del contaminante a tratar pues la cinética de la degradación de un compuesto aromáticos varia en relación a la de un alifáticos, poseen diferentes velocidades y mecanismos de reacción, además algunos hidrocarburos contienen dentro de ellos átomos de halógenos que presentan una fuerte toxicidad para ciertas familias del reino Monera inhibiendo su crecimiento [7].
El Estero Salado es un estuario icónico de la ciudad de Guayaquil, además de ser uno de los medios acuáticos más importantes del país, en el último medio siglo la contaminación continua ha provocado graves cambios tanto en aguas como en suelo perdiendo así su belleza natural. Para identificar las causas de dicha contaminación, medir los niveles de contaminantes, indagar sobre los efectos de la misma y buscar alternativas para remediar el daño causado, se han realizado numerosas investigaciones alrededor del tema [8].
Entre las investigaciones más recientes sobre los niveles de Hidrocarburos del Estero Salado está el estudio de las concentraciones por metales pesados e hidrocarburos en el ramal B del estero salado realizado por el Ingeniero Víctor Hugo Rivera Pizarro como trabajo de titulación para obtener el título de ingeniero químico donde los niveles de hidrocarburos se encontraban entre 800 y 1000 mg/Kg en 6 estaciones del tramo B, Otra investigación un poco más antigua es el estudio de los efectos de la contaminación hidrocarburifica en los macroinvertebrados del estero salado realizado por la Bióloga Maritza Cárdenas Calle como trabajo titulación de postgrado en la cual se especifica al sector Miraflores como la zona del tramo B con mayores niveles, alrededor de 1124 mg/Kg, mientras que en zonas como Kennedy y Urdesa se encuentra entre los 200 y 100 mg/Kg.
En cuanto a las causas Noelia Vascones en su trabajo de titulación señala como principales causas de la contaminación, el prácticamente nulo cumplimiento de las normativas ambientales por parte de las industrias ubicadas en el norte del Tramo B y la falta de sanciones y medidas de control más eficientes por parte de los organismos estatales y gobiernos seccionales. A pesar de ello también se habla sobre los avances que se han logrado en el sector sur del estero, específicamente los que forman parte del proyecto Guayaquil Ecológico, la reubicación de familias que Vivian en las riberas, a través del plan Socio Vivienda en coordinación con el MAE, reducción de malos olores en el tramo A aplicando super-oxigenacion, reforestación de las riberas en el sector el Cisne II. Se menciona que a partir del año 2007 la empresa VISOLIT S.A. ha participado y ganado todos los recursos para el mantenimiento del estero salado y posee contratos vigentes hasta el año 2019.
1.1. Composición del crudo de petróleo
El crudo de petróleo es un líquido negro y altamente viscoso formado por una alta variedad de sustancias orgánicas, pudiendo contener miles de compuestos, básicamente hidrocarburos (un 50-98% de la composición) [9]. Los hidrocarburos son utilizados para la producción de multitud de artículos, por lo que son uno de los grupos más importantes de contaminantes al medio ambiente, no solo por su abundancia, también por su persistencia en diferentes ecosistemas [10]. La mayoría de los hidrocarburos son n-alcanos o alcanos de cadena lineal también llamados parafinas, otros son alcanos ramificados (en menor cantidad), naftenos y diferentes cantidades de hidrocarburos aromáticos [11]. El crudo de petróleo posee una composición elemental mayoritariamente de carbono-hidrogeno de alrededor de 84-87% de C y 11-14% de H, además contiene de 0-8% de S, y de 0-4% de O y N y trazas de metales como el níquel, el vanadio entre otros [12].
1.2. Composición por familias de hidrocarburos
Para un estudio más detallado de los hidrocarburos provenientes del petróleo se suelen colocar los compuestos en familias:
Ø Parafinas volátiles (alcanos hasta C10),
Ø Parafinas no volátiles (alcanos entre C10-C40),
Ø Naftenos (ciclo alcanos)
Ø Olefinas (alquenos)
Ø Aromáticos (monoaromáticos y poliaromáticos).
Ø Resinas y los asfáltenos
1.3. Problemas socio ambiental generados por la industria petrolera
En la actualidad, los distintos países dependen del petróleo y sus productos; la estructura física y la forma de vida de las aglomeraciones periféricas que rodean las grandes ciudades son posibles gracias a un suministro de petróleo relativamente abundante y barato. Sin embargo, en los últimos años ha descendido la disponibilidad mundial de esta materia, y su costo relativo ha aumentado. Es probable que, a mediados del siglo XXI, el petróleo ya no se use comercialmente de forma habitual [13].
El suelo como hábitat para los microorganismos
Llamamos suelo a la parte más externa de la corteza terrestre, resultante de la meteorización de las rocas subyacentes y con unas características claramente diferenciadas de las mismas. Podemos considerar el suelo como un sistema de interacción entre tres fases bien definidas: una fase sólida, constituida por materia mineral y orgánica, una fase líquida, y una fase gaseosa o atmósfera del suelo [14].
El tipo y composición de la materia mineral viene dado por las características de las rocas del subsuelo, así como de los procesos edáficos que hayan tenido lugar en su formación. La porción inorgánica es muy importante por su influencia en la disponibilidad de nutrientes, aireación, retención de agua, etc. La materia orgánica procede de la actividad de los distintos organismos vivos del suelo y su composición y cantidad es variable, principalmente en función del tipo de cubierta vegetal. El resto del volumen del suelo está prácticamente constituido por espacios porosos, que a su vez están ocupados por agua y los gases que constituyen la atmósfera edáfica [15]. La porosidad (cantidad y tamaño de los poros) depende de la textura, determinada por la cantidad de arena, limo y arcilla, la estructura y el contenido en materia orgánica. Todos estos factores determinan a su vez el movimiento y capacidad de retención de agua del suelo y la composición gaseosa de su atmósfera. De forma característica la atmósfera del suelo se encuentra enriquecida en dióxido de carbono y empobrecida en oxígeno, como resultado de la respiración aeróbica de raíces de plantas, animales y microorganismos. Sin embargo, cuando se producen condiciones de anaerobiosis (por acumulación de agua en los poros del suelo) aparecen en la atmósfera del suelo otros gases como óxido nitroso, nitrógeno gaseoso y metano, resultantes de actividad respiratoria anaeróbica bacteriana. Tanto el contenido en agua como la composición de la atmósfera del suelo son factores que fluctúan ampliamente [16].
Este sistema complejo que constituye el suelo, característicamente heterogéneo espacial y temporalmente, alberga una gran riqueza de especies vegetales, animales y microbianas. El suelo es un ambiente muy apropiado para el desarrollo de los microorganismos tanto eucariotas (algas, hongos, protozoos) como procariotas (bacterias y arqueas). También encontramos virus y bacteriófagos. Todos estos organismos establecen relaciones entre ellos en formas muy variadas y complejas y también contribuyen a las características propias del suelo por su papel en la modificación de las fases sólida, líquida y gaseosa antes mencionadas. Los microorganismos desempeñan funciones de gran importancia en relación con procesos de edafogénesis; ciclos biogeoquímicos de elementos como el carbono, el nitrógeno, oxígeno, el azufre, el fósforo, el hierro y otros metales; fertilidad de las plantas y protección frente a patógenos; degradación de compuestos xenobióticos, etc [17].
Los organismos del suelo no se distribuyen al azar, sino que siguen patrones espaciales de agregación, a escalas diferentes (desde nm a km) que se superponen. Esta estructuración obedece al efecto causado por diferentes factores de control y es totalmente dinámica. Utilizando técnicas de observación de secciones ultrafinas de suelo mediante microscopía electrónica, tomografía, análisis geoestadístico y la elaboración de modelos, se ha demostrado que la distribución de las bacterias edáficas. Está altamente estructurada, y que esta estructuración es importante para la funcionalidad del suelo. Las bacterias se organizan en microcolonias compuestas de pocas células que pueden pertenecer a diferentes morfotipos. Factores como la presencia de raíces, pequeños agregados, nutrientes y poros parecen gobernar la distribución de bacterias en microhábitats [18].
La complejidad del suelo como ecosistema (nivel microscópico incluido) junto con las especiales particularidades de los microorganismos, tales como su tamaño microscópico y las dificultades para una diferenciación basada en su morfología, habían proporcionado una visión del mundo microbiano edáfico como una “caja negra” de la cual se sabía que cumplía una función, aunque no se conociese su contenido [19].
1.4. Factores que influyen la Biorremediación
La concentración y composición de la comunidad microbiana y la tasa de transformación de contaminantes está influenciada por diversos factores:
Ø Necesidad de nutrientes: El metabolismo microbiano está orientado a la reproducción de los organismos y éstos requieren que los constituyentes químicos se encuentren disponibles para su asimilación y sintetización. Los nutrientes principalmente requeridos son el fósforo y el nitrógeno. Por lo general suele haber en el suelo una concentración de nutrientes suficiente, sin embargo, si estos no se encontrasen en el rango normal se puede adicionar mayor cantidad al medio. El rango normal de C: N: P depende del sistema de tratamiento a emplear, siendo de modo habitual 100:10:1.
Ø pH del suelo: afecta significativamente en la actividad microbiana. El crecimiento de la mayor parte de los microorganismos es máximo dentro de un intervalo de pH situado entre 6 y 8. Así mismo el pH también afecta directamente en la solubilidad del fósforo y en el transporte de metales pesados en el suelo. La acidificación o la reducción del pH en el suelo se puede realizar adicionando azufre o compuestos del azufre.
Ø Humedad: los microorganismos requieren unas condiciones mínimas de humedad para su crecimiento. El agua forma parte del protoplasma bacteriano y sirve como medio de transporte a través del cual los compuestos orgánicos y nutrientes son movilizados hasta el interior de las células. Un exceso de humedad inhibirá el crecimiento bacteriano al reducir la concentración de oxígeno en el suelo. El rango varía en función de la técnica.
Es el resultado de los procesos de digestión, asimilación y metabolización de un compuesto orgánico llevado a cabo por bacterias, hongos, protozoos y otros organismos [20].
Los microorganismos del terreno transforman tanto compuestos orgánicos como inorgánicos. Los procesos de biodegradación incluyen reacciones de oxidación-reducción, procesos de adsorción e intercambio de iones y reacciones de quelación de formación de complejos, que dan lugar a la fijación de los metales [21].
Muchos estudios han demostrado que la biodegradación por los microbios indígenas puede contribuir perceptiblemente a la destrucción de compuestos orgánicos
La biodegradación es un proceso natural ventajoso no sólo por permitir la eliminación de compuestos nocivos impidiendo su concentración, sino que además es indispensable para el reciclaje de los elementos en la biosfera, permitiendo la restitución de elementos esenciales en la formación y crecimiento de los organismos (carbohidratos, lípidos, proteínas). La descomposición puede llevarse a cabo en presencia de oxígeno (aeróbica) o en su ausencia (anaeróbica). La primera es más completa y libera energía, dióxido de carbono y agua, es la de mayor rendimiento energético y se describe así:
Degradación aerobia
![]()
La biodegradación aerobia es la reacción más fácil para la aceptación de electrón terminal y esta usada para la biodegradación de los hidrocarburos del petróleo. Este proceso de degradación ocurre en presencia de microbios aerobios. Los últimos productos de la mineralización de compuestos orgánicos son dióxido de carbono, agua y masa de la célula. Los organismos anaerobios facultativos pueden utilizar el oxígeno cuando es presente o puede cambiar en aceptadores alternativos del electrón.
Los procesos anaeróbicos son oxidaciones incompletas y liberan menor energía y se describen así:
Degradación anaerobia
![]()
Otros aceptadores de electrón como los iones nitrato, sulfato, férrico, manganeso, y así sucesivamente, serán utilizados cuando el oxígeno no está disponible. Es obligar los organismos anaerobios a ser dominante en ausencia del oxígeno [22]. La degradación bajo condiciones anaerobias puede ser relativamente lenta. Los productos metabólicos de la biodegradación anaerobia incluyen los ácidos orgánicos simples, el CO2, el H2O, el CH4, el H2, el N2, y la masa de la célula [23].
En la ciudad de Guayaquil el Estero Salado representa un sistema estuarino icónico de la metrópolis, se extiende alrededor de 60 Km desde el Puerto Marítimo hasta Posorja, formando parte del Golfo de Guayaquil.
Este ecosistema estuarino brinda una diversidad de recursos y servicios ecológicos significativos y valiosos para la sustentación de la metrópolis de Guayaquil, albergando una amplia variedad de empresas del sector acuícola, el cual es parte importante de la economía no petrolera del país, lo cual sustenta su amplio de valor ecológico y comercial [20].
Existen áreas delimitadas para un manejo sustentable de los recursos del Estero Salado, como:
Ø Bosque Protector Salado del Norte de (47,23 hectáreas)
Ø Bosque Protector Puerto Hondo (2.000 hectáreas)
Ø Reserva de Producción Faunística Manglares el Salado con (5.409 hectáreas).
Sin embargo, al encontrarse situada en la ciudad más poblada del país [A9], el estuario del Estero Salado está siendo perjudicado en diferente forma por diferentes causas antropogénicas que se realizan en la ciudad y en sus periferias. Si a esto agregamos, que el aumento acelerado de la población en la urbe y el crecimiento inmediato del perímetro urbano que esto conlleva han dado lugar a asentamientos urbanos ilegales y no planificados por las autoridades causando que tengan sistemas de alcantarillado insuficientes, sin ningún tipo de tratamiento en sus aguas residuales y realicen la disposición final de sus desechos sólidos en el estuario [24].
De las aguas residuales con poco o ningún tratamiento que ingresan continuamente a los diferentes ramales del Estero, alrededor de un 60% corresponden a uso doméstico y un 40% corresponde a uso industrial [25].
Al mismo tiempo que esto ocurre ingresan contaminantes de forma discontinua, por las escorrentías correspondientes a zonas de cultivo y usufructo de recursos minerales en canteras situadas en los alrededores periféricos de la metrópoli, además de desechos hidrocarburiferos, lixiviados derivados de desechos sólidos domésticos e industriales por escorrentías procedentes de superficies no permeables [26].
El Estero Salado, por ser un brazo de mar, y al no recibir aportes de afluentes o ríos situados aguas arriba, sus aguas tienen cierto movimiento que no está dirigido predominantemente hacia el mar abierto; el cuerpo de agua se desliza con la marea hacia el mar, pero recupera aguas residuales con poco o ningún tratamiento, ingresan de manera puntual a los diferentes ramales del Estero, cerca de un 60% correspondiente a uso doméstico y 40% de uso industrial [24]. Adicionalmente, ingresan contaminantes de manera no puntual, por las escorrentías provenientes de zonas de cultivo y explotación de canteras ubicadas en la periferia de la ciudad, además de basura, lixiviados y contaminantes por escorrentías provenientes de superficies no permeables (techos, puentes, calles, aceras) [25].
Este brazo de mar, y al no estar conectado a otros afluentes o ríos situados aguas arriba y gracias a que sus aguas poseen cierto movimiento que no está encaminado preferentemente hacia el mar abierto; el cuerpo de agua se desplaza con la marea hacia el mar, pero recobra su estado originario con el descenso de la misma; este proceso perturba la renovación y hace mucho más difícil la autodepuración de las aguas en el estuario del Estero Salado, fundamentalmente hacia las zonas más periféricas de la ciudad de Guayaquil [27].
Si a lo antes mencionado adicionamos el hecho que las zonas intermareales demuestran una respuesta inmediata a todas estas alteraciones de los ecosistemas colindantes a la zona intermareal [25].
Este efecto ha influenciado de una manera u otra al detrimento de la calidad ambiental, estética y productiva del estuario, perjudicando:
Ø La actividad económica en la zona impidiendo la explotación de sus recursos pesqueros y deteriorando la calidad del agua para el uso de la industria camaronera que es tomada de los ecosistemas cercanos [28].
Ø Como a un abundante número de especies que conviven en el estuario, destruyendo paulatinamente este ecosistema [26].
2. Materiales y métodos
La investigación fue desarrollada en los meses de agosto del 2018 a febrero del 2019, durante periodos de marea baja, comprobadas en las tablas de marea del INOCAR.
Mencionado por la Municipalidad de Guayaquil, los sectores a estudiarse según estudios ambientales realizados esta es una de las zonas con mayor afectación de contaminación hidrocarburifica debido a la emisión de aguas residuales de uso doméstico de las urbanizaciones aledañas y de desechos industriales [29].

Fig. 1. Fotografía de la zona de muestra Miraflores
Fuente: Elaboración propia
Las muestras del suelo se tomaron entre los 20 y 35 cm de profundidad y se almacenaron sobre bandejas de aluminio y se dejaron secar a temperatura ambiente por 48 horas.
Se trabajó con tres tratamientos y dos réplicas de cada una, en dos zonas del estero salado de la Ciudad de Guayaquil, se almacenaron las muestras a temperatura ambiente durante 48 horas [29].
2.1. Hidrocarburos totales de petróleo
Procedimiento
Ø Se marca el recipiente de la muestra para determinar posteriormente el volumen de la muestra. Si la muestra no se acidificó al momento de la recolección, agregue 5 ml de ácido clorhídrico a el recipiente de muestra.
Ø Después de mezclar la muestra, se verifica el pH tocando el papel sensible al pH en la tapa para asegurarse de que el pH sea 2 o inferior.
Ø Se añade más ácido si es necesario.
Ø Se vierte la muestra en un embudo de separación. agregando 30 ml de fluorocarbono-113 a el recipiente de muestra y se gira para enjuagar los lados. Se transfiere el solvente al embudo de separación. Extrayendo mediante agitación vigorosamente durante 2 minutos. Permitiendo que las capas se separen.
Ø Se filtra la capa de solvente a través de un embudo que contiene papel de filtro humedecido con solvente en un matraz volumétrico de 100 ml.
Ø NOTA 1: Una emulsión que no se disipa puede romperse vertiendo aproximadamente 1 g de sulfato de sodio en el cono del papel de filtro y drenando lentamente la emulsión a través de la sal. Se pueden agregar también porciones de 1 g adicionales al cono según sea necesario.
Ø Se repiten los dos pasos anteriores dos veces más con porciones de 30 ml de solvente nuevo, combinando todo el solvente en el matraz volumétrico.
Ø Se enjuaga la punta del embudo de separación, el papel de filtro y el embudo con un total de 5-10 ml de disolvente y se recogen los enjuagues en el matraz. Diluyendo el extracto a 100 ml. Si se sabe que el extracto contiene más de 100 mg de material orgánico no hidrocarbonado,
Ø Pipeteamos una porción apropiada de la muestra a un volumen volumétrico de 100 ml y se diluye al volumen.
Ø Desechamos alrededor de 5-10 ml de solución del matraz volumétrico. Añadiendo 3 g de gel de sílice y una barra de agitación; se tapa el matraz volumétrico y agitando la solución durante un mínimo de 5 minutos con un agitador magnético.
Ø Se calibra el instrumento para las celdas apropiadas utilizando una serie de estándares de trabajo. No es necesario agregar gel de sílice a los estándares.
Ø Determinamos la absorbancia directamente para cada solución en el máximo de absorbancia a aproximadamente 2930 cm-1.
Ø Preparamos un gráfico de calibración de absorbancia vs. mg de petróleo.
Ø Hidrocarburos por 100ml de solución.
Ø Después de que el gel de sílice se haya asentado en el extracto de la muestra, llenamos una celda limpia con solución y determinamos la absorbancia del extracto. Si la absorbancia excede
Ø 0.8 preparar una dilución apropiada.
Ø NOTA 2: La posibilidad de que se haya excedido la capacidad de absorción del gel de sílice se puede probar en este punto agregando otros 3.0 g de gel de sílice al extracto y repitiendo el tratamiento y la determinación.
Ø Determinamos la concentración de hidrocarburos del petróleo en el extracto comparando la respuesta con el gráfico de calibración [27].
De cada una de las muestras, se tomaron 100 g de muestra de suelo.
Las muestras fueron puestas en una bandeja de aluminio y se adicionaron 25 ml de NaOH (0,1 N) en la superficie de la bandeja y cubiertas por un vaso de precipitación, se dejaron a temperatura ambiente durante 48 horas , se utilizó fenolftaleína como indicador y se realizó la titulación con HCl 0,1 N.
3. Resultados
3.1. Resultados experimentales y análisis de resultados
Los niveles de Potencial de Hidrogeno de los sedimentos obtenido muestran niveles ligeramente alcalinos de alrededor de 8 antes de aplicar el tratamiento, siendo la estación de Miraflores la más alcalina. Después del tratamiento los niveles de pH se reducen en todos los Sedimentos, llegando a niveles neutros de 7 unidades de pH y ligeramente ácidos de 6,8 niveles de pH, el mayor cambio se presenta en la Toma C del Sector Miraflores donde cae de 8,86 a 6,85 Y el menor en la Toma C del Sector del Puente Zig Zag.
Tabla 1.
Resultados de pH
|
Muestra |
Antes |
Después |
Toma |
|
Miraflores |
8,7 |
7 |
A |
|
Miraflores |
8,58 |
7,02 |
B |
|
Miraflores |
8,86 |
6,85 |
C |
|
Puente Zig Zag |
8,08 |
6,85 |
A |
|
Puente Zig Zag |
7,87 |
7 |
B |
|
Puente Zig Zag |
7,55 |
6,24 |
C |
Fuente: Elaboración propia
En la siguiente figura 2 podemos apreciar de mejor manera el cambio en los niveles de pH de cada tratamiento, apreciando que tanto en el Sector Miraflores como en el Sector del Puente Zig Zag el cambio en el pH tiende a un valor siempre muy cercano al neutro absoluto.
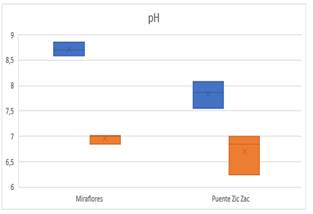
Fig. 2. Cambios de pH
Fuente: Elaboración propia
Se observa que la reducción de pH en los tratamientos del Sector Miraflores es alrededor de 2 y en el Sector del puente Zigzag de 1, siendo la disminución promedio en los niveles de pH después del tratamiento de alrededor 1,44 con una desviación estándar de 0,4.
Todas estas afirmaciones serán comprobadas mediante el uso de modelos estadísticos, demostrando o desmintiendo cada hipótesis que podamos cuantificar.
Con el resultado obtenido al restar el peso del recipiente del alcanzado por la muestra seca en el recipiente, calculamos el porcentaje de Humedad:
|
|
( 1) |
Los resultados conseguidos se muestran en la siguiente Tabla 2:
Tabla 2.
Resultados de humedad
|
ANTES |
DESPUÉS |
||||
|
Gr de muestra seca |
% Humedad |
Gr de muestra seca |
% Humedad |
Diferencia |
|
|
A1 |
28 |
53,33 |
48 |
20 |
20 |
|
B1 |
14 |
76,66 |
40 |
33,33 |
26 |
|
C1 |
13 |
78,33 |
38 |
36,66 |
25 |
|
A2 |
25 |
58,33 |
46 |
23,33 |
21 |
|
B2 |
28 |
53,33 |
37 |
38,33 |
9 |
|
C2 |
34 |
43,33 |
36 |
40 |
2 |
Fuente: Elaboración propia
Como podemos observar en la siguiente [28], como los porcentajes de Humedad en un inicio son mayores en Miraflores(azul) donde alcanza un promedio de 69,44%, mientras en el Sector del Zig Zag la humedad promedio es del 51,66%.

Fig. 3. Comportamiento de humedades (antes)
Fuente: Elaboración propia
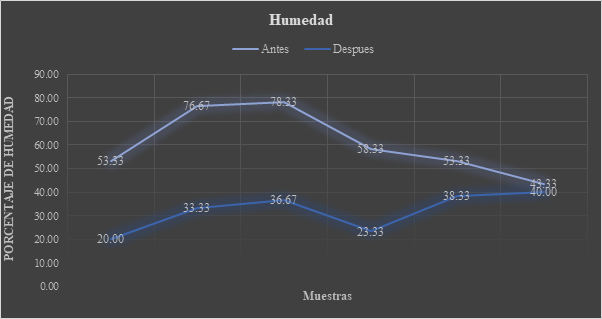
Fig. 4. Comportamiento de humedades (después)
Fuente: Elaboración propia
La Desviación de los resultados de humedad antes del tratamiento es menor en el Sector del Puente Zig -Zag.
Tabla 3.
Resultados de humedad
|
Parámetro |
Total |
Zig Zag |
Miraflores |
|
Promedio |
60,555556 |
51,6666667 |
69,4444444 |
|
Desviación |
14,010578 |
7,63762616 |
13,9774951 |
Fuente: Elaboración propia
Al tratarse de lodos sedimentarios que se encuentran en el fondo del Estero Salado, es comprensible que el agua alcance alrededor de dos terceras partes de su composición.
La reducción en la humedad pueda deberse al cambio de condiciones que experimento la muestra desde la rivera del estero al laboratorio, o a los cambios fisicoquímicos que se producen como efecto del incremento poblacional de los consorcios bacterianos.
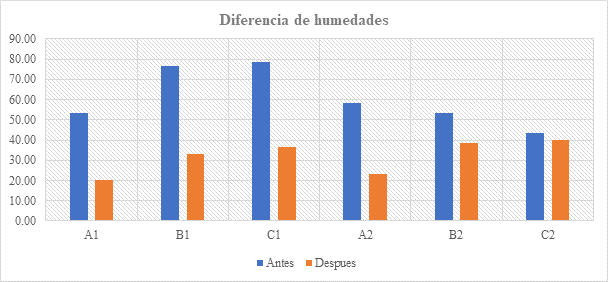
Fig. 5. Diferencias de humedades
Fuente: Elaboración propia
Al obtener los ml de Ácido Clorhídrico 0.1 N necesarios para neutralizar la solución se utilizó la siguiente fórmula:
|
|
( 2) |
Obteniendo de ella los moles de CO2 producidos en cada caso, en la siguiente Tabla 4 Tabla 4 pueden observar los valores obtenidos:
Tabla 4.
Valores obtenidos para el CO2
|
ml ClH |
1 |
2 |
molC02 |
1 |
2 |
|
A |
40 |
39 |
A |
0,001 |
0,0011 |
|
B |
43 |
42 |
B |
0,0007 |
0,0008 |
|
C |
42 |
40 |
C |
0,0008 |
0,001 |
Fuente: Elaboración propia
Con los valores obtenido en mol CO2 se obtuvo las partes por millón de carbono perdidos en las muestras obteniendo lo mostrado en la tabla 5
|
|
( 3) |
Tabla 5.
Ppm de Carbono
|
Ppm C/muestra |
1 |
2 |
|
A |
151,260504 |
166,386555 |
|
B |
105,882353 |
121,008403 |
|
C |
121,008403 |
151,260504 |
Fuente: Elaboración propia
La figura 6 ppm (carbono)representa los valores obtenidos en cada caso:
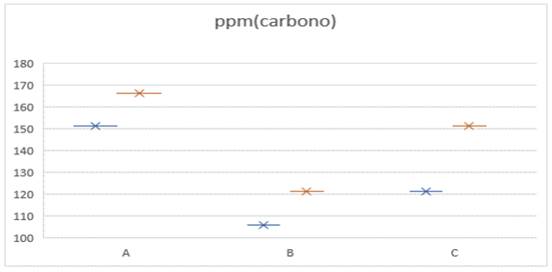
Fig. 6. Comportamiento de la producción de carbono
Fuente: Elaboración propia
El promedio de partes por millón de carbono consumido por las bacterias en 15 días fue de 136,13 ppm Tabla 6, lo que da una razón de 9 ppm/día aproximadamente.
Tabla 6.
Promedios de ppm de carbono
|
Parámetro |
Total |
Zigzag |
Miraflores |
|
Promedio |
136,134454 |
146,218487 |
126,05042 |
|
Desviación |
14,2609771 |
23,1054237 |
23,1054237 |
Fuente: Elaboración propia
Los datos obtenidos de este experimento fueron comparados con los alcanzados en las pruebas de concentración de Hidrocarburos Totales de Petróleo, para comprobar que la reducción en dichas concentraciones se debe a una degradación, llevada a cabo por los consorcios bacterianos utilizados; o se debe a algún otro factor.
Ø Los lodos sometidos al tratamiento redujeron sus niveles de pH entre 1 y 2 puntos desde ligeramente alcalino hasta ligeramente ácido y neutro sin excepción alguna.
Ø La disminución en los niveles de pH en ambos Sectores es prácticamente el mismo y poseen una Humedad similar, por lo que se podría concluir que las características fisicoquímicas medidas en ambos tipos de suelos son idénticos.
Ø Los lodos sometidos al tratamiento redujeron su humedad en diferentes proporciones sin excepción alguna, pero la eficiencia varia significativamente, por lo cual podríamos concluir que las condiciones entre fueron diferentes entre los diferentes métodos.
Ø En las pruebas de CO2 se logró corroborar que la metabolización de Carbono es similar en todos los casos con un promedio de 9±0,63 ppm/día.
Ø Los Consorcios bacterianos metabolizaron el carbono de los Hidrocarburos presentes en la muestra, reduciendo los niveles de concentración de TPH y generando CO2 como desecho.
Ø La reducción en las concentraciones de TPH nos permite concluir que ocurre una degradación de los hidrocarburos alifáticos.
Ø La producción de CO2 en las trampas de respirometria permite concluir que las bacterias metabolizan el carbono que obtienen de las fuentes del suelo, entre estas fuentes el TPH que se degrado.
Referencias.
|
[1] |
M. C. Cárdenas Calle, «Efecto de la contaminación hidrocarburífera sobre la estructura comunitaria de macroinvertebrados bentónicos presentes en el sedimento del Estero Salado,» Universidad de Guayaquil, Guayaquil, 2010. |
|
[2] |
E. P. Rodríguez Ochoa, «Biorremediación de los suelos contaminados con hidrocarburos provenientes de la Estación de Secoya utilizando un consorcio bacteriano aerobio a escala de laboratorio.,» Escuela Superior Politécnica de Chimborazo, Chimborazo, 2018. |
|
[3] |
O. H. Pucci, M. A. Bak, S. R. Peressutti, I. Klein, C. Härtig, M. H. Álvarez y L. Wünsche, «Influence of Crude Oil Contamination on the Bacterial Community of Semiarid Soil of Patagonia,» Enginnering, vol. 20, nº 2, pp. 129-146, 2004. |
|
[4] |
O. H. PUCCI, A. ACUÑA y G. N. PUCCI, «Biodegradación de residuos de estaciones de servicio y lavaderos industriales por la cepa Rhodococcus erythropolis,» Acta Biológica Colombiana, vol. 18, nº 2, 2013. |
|
[5] |
V. I. Prieto Díaz y A. Martínez de Villa Pérez, «La contaminación de las aguas por hidrocarburos: un enfoque para abordar su estudio,» Revista Cubana de Higiene y Epidemiología, vol. 37, nº 1, 1999. |
|
[6] |
J. O. M. G. A. M. S. y. J. A. Grimalt, «Microbial degradation of marine evaporitic crude oils.,» 1991. |
|
[7] |
S. R. Peressutti, H. M. Alvarez y O. H. Pucci, «Dynamics of Hydrocarbon-Degrading Bacteriocenosis of an Experimental Oil Pollution in Patagonian Soil,» International Biodeterioration & Biodegradation, vol. 52, nº 1, pp. 21-30, 2003. |
|
[8] |
J. M. A. A. M. S. R. P. P. G. y. M. E. Bayona, «Selective aerobic degradation of methyl-substituted polycyclic aromatic hydrocarbons in petroleum by pure microbial cultures.,» Int. J. Environ. Anal. Chem., 1986. |
|
[9] |
L. F. Barrios-Ziolo, J. Robayo-Gómez, S. Prieto-Cadavid y S. A. Cardona-Gallo, «Biorremediación de Suelos Contaminados con Aceites Usados de Motor,» Cintex, vol. 20, nº 1, 2015. |
|
[10] |
P. M. Chapman y F. Wang, «Assessing sediment contamination in estuaries,» Environmental Toxicology and Chemistry, vol. 20, nº 1, 2009. |
|
[11] |
V. H. Rivera Pizarro, «Estudio de las concentraciones por Metales Pesados e Hidrocarburos en el Ramal B Del Estero Salado,» Universidad de Guayaquil, 2016. |
|
[12] |
A. O. Ameh, I. A. Mohammed-Dabo, S. Ibrahim, J. B. Ameh, C. D. Azienge y Y. Tanimu, «Earthworm survival in used engine oil contaminated soil spiked with manure,» International Journal of Biological and Chemical Sciences, vol. 5, nº 3, 2011. |
|
[13] |
J. W. a. R. Colwell, «Microbial petroleum degradation; uses of mixed hydrocarbon substrate,» 1974. |
|
[14] |
J. Pinedo Alonso, «Evaluación de riesgos en suelos afectados por hidrocarburos de petróleo,» UNIVERSIDAD DE CANTABRIA, 2014. |
|
[15] |
A. MARTÍNEZ–PRADO, M. E. PÉREZ–LÓPEZ, J. PINTO–ESPINOZA, B. A. GURROLA–NEVÁREZ y A. L. OSORIO–RODRÍGUEZ, «Biorremediación de suelo contaminado con hidrocarburos empleando lodos residuales como fuente alterna de nutrientes,» Revista internacional de contaminación ambiental, vol. 27, nº 3, 2011. |
|
[16] |
S. J. Ergas, D. P. Chang, E. D. Schroeder y J. B. Eweis, Bioremediation Principles., Malaysia: Mc Graw Hill,, 1998. |
|
[17] |
C. H. Ettema y D. Wardle, «Spatial Soil Ecology,» Trends in Ecology & Evolution, vol. 17, nº 4, pp. 177-183, 2002. |
|
[18] |
N. Nunan, K. Wu, I. M. Young, J. W. Crawford y K. Ritz, «Spatial Distribution of Bacterial Communities and Their Relationships with the Micro-structure of Soil,» FEMS Microbiol Ecol, vol. 44, nº 2, p. 203, 2003. |
|
[19] |
H. Insam, «Developments in soil microbiology since the mid 1960s,» Geoderma, vol. 100, nº 3-4, pp. 389-402, 2001. |
|
[20] |
D. W. Pritchard, What is an estuary: Physical Viewpoint, Washington, DC,: American Association for the Advancement of Science,, 19676. |
|
[21] |
J. D. Walker y R. R. Colwell, «Microbial petroleum degradation; uses of mixed hydrocarbon substrate,» Appl Microbiol., vol. 27, nº 6, p. 1053–1060., 1974. |
|
[22] |
W. Ayarza, S. Coello, N. Chalén de Padilla, P. Garcés, L. García, M. L. García, F. Ormaza, E. Pérez, F. Pesantes y L. Solórzano, «Estudios Geobioquímicos de la Sección Urbana del Estero Salado,» Revista de Ciencias del Mar y Limnología, vol. 3, nº 1, 1993. |
|
[23] |
J. G. Chan Quijano, «Evaluación de la degradación de hidrocarburos totales del petróleo por bioestimulación con abonos orgánicos asociados a especies arbóreas,» ECOSUR, Tabasco, 2015. |
|
[24] |
L. Solórzano y G. Viteri, «Investigación Química del Estero Salado,» Revista de Ciencias del Mar y Limnología, vol. 3, nº 1, 1993. |
|
[25] |
S. R.-D. R. y R. Castro-Rendón, «Niveles de cadmio en peces de alto consumo de aguas continentales en la Provincia de los Ríos, Ecuador,» Ciencias Naturales y Ambientales, vol. 13, nº 2, 2019. |
|
[26] |
A. C. De la parra y C. A. García-Alzate, «Metabolismo de un tramo en la cuenca baja del río Cesar, departamento del Cesar, en una época de sequía, Colombia,» Intropica, vol. 14, nº 1, pp. 16-23, 2019. |
|
[27] |
J. Negrete, J. Varela, E. Heras y M. Alcívar, Plan de Recuperación del Estero Salado primera parte., Guayaquil: Universidad Especialidades Espiritu Santo, 2019. |
|
[28] |
M. Cárdenas y J. Mair, «Caracterización de macroinvertebrados bentónicos de dos ramales estuarinos afectados por la actividad industrial, Estero Salado-Ecuador,» Intropica, vol. 9, nº 1, p. 118–128, 2015. |
|
[29] |
A. J. Quinteros, J. Castro Salcedo y F. León, «LA RESERVA DE PRODUCCIÓN FAUNÍSTICA MANGLARES EL SALADO (RPFMS) DE GUAYAQUIL, COMO RECURSO TURÍSTICO SOSTENIBLE,» Revista Caribeña de Ciencias Sociales, vol. 14, nº 1, 2017. |