1. Introducción
Desde la antigüedad las plantas son utilizadas en varias partes del mundo por sus propiedades nutritivas, medicinales, aunque el empleo de las plantas con fines terapéuticos estuvo durante muchos años asociado a ritos atractivos y religiosos, en tal caso el resaltar la utilización para su posterior conocimiento ancestral de las plantas. El origen de la utilización de las esencias y aromas es tan antiguo como la agricultura. Comenzó por la observación y recolección de plantas que eran aprovechadas por los animales, pasando a una recolección selectiva de las mejores características organolépticas como el sabor del fruto, tamaño y aroma hasta llegar a domesticar las plantas más útiles hasta su extensión a cultivo. [1]
Las plantas hoy en día se aprovechan en la industria alimentaria, medicina, cosméticos entre otros. En los últimos años se ha estudiado el efecto de los compuestos bioactivos presentes en las plantas para ser utilizados en la medicina, por lo cual existe varios reportes sobre sus propiedades funcionales, medicinales y/o toxicológicas [1]. Sin embargo, lo que se conoce de las plantas y sus compuestos bioactivos es muy bajo para el potencial que nos pueden aportar en el desarrollo de nuevos compuestos. [1] Diversas fuentes investigativas indican que los subproductos más importantes del romero son su extracto acuoso y aceite esencial. [2]. En los últimos años se han extendido una gran cantidad de aportaciones científicas que brindan una amplia información acerca de las aplicaciones del romero. [3]
Tomando en consideración que al sintetizar nanopartículas de plata mediante métodos físicos y químicos tienen un gran impacto ambiental y económico. En la actualidad se están realizando investigaciones, que sean de gran beneficio para el medio ambiente conocidos como síntesis verde, eficientes y que sean más factibles produciendo menor cantidad de residuos contaminantes que en otros métodos ya utilizados. [4]
La nanotecnología al ser implementada en el uso de diversas ramas aplicativas como en la medicina, en la industria textil, en la agricultura, etc.; así mismo en la actualidad existen algunas investigaciones que se han realizado utilizando nanopartículas de plata a partir de extractos de plantas. [5]
Existen algunos reportes que se han realizado acerca de la síntesis de nanopartículas de plata a partir de las cáscaras de algunas frutas como puede ser el banano, etc.; así también en plantas de ajo, sábila, albahaca, mático, cilantro, y romero que poseen componentes bioactivos con contenido antimicrobiano de forma natural de acuerdo con sus propiedades son capaces de producir una reducción en la plata y sintetizar nanopartículas [6]. Extractos de plantas como el romero (Rosmarinus Officinalis) han demostrado en varios estudios que poseen una gran variedad de compuestos y propiedades antioxidantes y antimicrobianas utilizadas como medicina ancestral [7].
También existen varios reportes donde se han realizado investigaciones acerca de los compuestos del romero presenciando metabolitos secundarios y aceites esenciales, algunos compuestos que contiene el romero son flavonoides, terpenos, ácidos fenólicos entre otros [3]
En relación con las especificaciones descritas con anterioridad, en este trabajo de titulación propone sintetizar nanopartículas de plata a partir del extracto de las hojas de romero debido a sus diversas propiedades que contienen como son los compuestos polifenólicos (CPF), los cuales son los principales responsables reductores y de gran importancia para el desarrollo de las nanopartículas.
En la actualidad ha aumentado enfermedades de origen microbiológica y esto se debe a la resistencia de ciertos microorganismos patógenos, a los antibióticos convencionales que son utilizados como aditivos en la industria alimentaria, que en numerosos informes son considerados como responsables de ser cancerígenos y teratogénicos por su toxicidad residual. Por esta causa, ha aumentado la tendencia al uso de conservantes de origen natural, y como resultado han ganado espacio entre el mercado al ser considerados como una alternativa viable en sustancias con actividad antimicrobiana. [3]
También, estudios previos informan que el extracto de la hoja de (Rosmarinus officinalis) presenta actividad antimicrobiana, aunque son muy escasos los trabajos realizados sobre la Concentración Inhibitoria Mínima (CIM) del mismo modo se observa que las cantidades de seres no visibles evaluados. La determinación del CIM es fundamental para evaluar las acciones de sustancias no tradicionales, y a su vez demostrar los valores de la inhibición de los patógenos teniendo en cuenta la alteración de sus características o parámetros a conservar. [2]
El romero (Rosmarinus officinalis L.) es conocida desde la antigüedad como una planta aromática, sus usos van desde fines medicinales además de ser utilizada como un valioso condimento, se deriva del griego “rhops y myrinos” que tiene como significado “arbusto marino” esto se debe al crecimiento cercano a la región costa. La planta de romero ha sido un peso importante debido a su trascendencia por las características medicinales que esta posee el mimo es de gran beneficioso para la humanidad y su cultura. [8]
El ser humano ha tenido desde hace miles de años una estrecha relación con las plantas, esto se debe al importante uso principalmente medicinal. Estas plantas han sido muy importantes para el desarrollo de medicamentos naturales y alimentos funcionales, ya que son una fuente importante de compuestos bioactivos. La investigación de las propiedades del romero tanto como sus aplicaciones viene asentada desde muchos años atrás, además de tener una ubicación geográfica muy beneficiosa para su fácil consumo y estudios es decir de fácil acceso, su plantación se extiende por las costas de todo el mundo, dentro de los subproductos más importantes del romero y que a su vez han sido de gran beneficio dándoles valor agregado entre estos se encuentra el extracto acuoso y aceite esencial. [9]
En el año de 1330 fue obtenido por primera vez el aceite esencial de romero por Ramón Llull desde aquel entonces, se lo emplea en perfumería. Según [9] expresa, que esta planta la usaban como un aromatizante natural, actualmente industrias han tomado en cuenta estas ideologías, para crear productos con el fin de satisfacer necesidades, por eejemplo,es utilizado en la industria farmacéutica esto se debe al ser considerado medicinal, así mismo usado para calmar malestares provocados por la ingesta de alimentos en mal estado, la industria de alimentos lo usa como un aromatizante y saborizante. [9]
La Fitoterapia es el nombre que le aplica al uso de plantas con el fin terapéutico esta ciencia estudia la utilización de las plantas medicinales con el objeto de prevenir, aliviar o curar enfermedades. Investigaciones indican que desde la antigüedad las hierbas han sido uno de los principales remedios curativos empleados por el hombre. No obstante, actualmente la fitoterapia es una alternativa que complementa a determinados tratamientos. [10]
La especie vegetal (Rosmarinus officinalis), perteneciente a la familia (Lamiaceae) conocida popularmente como romero, es una planta originaria de la región mediterránea, cultivada en muchos países del mundo y es utilizada como condimento y aromatizante en la elaboración de algunos alimentos, ya que es rica en principios activos que actúan en la mayoría de los órganos del cuerpo humano [3]. Contiene fuentes de metabolitos secundarios y aceites esenciales, algunos compuestos activos contenidos en el romero están distribuidos en flavonoides, terpenos, ácidos fenólicos seguidos de otros grupos funcionales. [3] Como subproductos de mayor relevancia están los de extracto entre ellos el acuoso y el aceite esencial. [2]. Además, es usada en la medicina tradicional por sus efectos digestivos, antiespasmódicos y carminativos. Últimamente se han extendido una gran cantidad de aportaciones científicas que brindan una amplia información acerca de las aplicaciones del romero. [3]
Su origen data en la región mediterránea del Sur de Europa y del Norte de África, el romero crece de manera espontánea o en cultivos. Por lo general se lo puede encontrar en las islas Baleares y en la Península a excepción del Norte su mayor producción es en las tierras bajas de clima cálido. Actualmente se cultiva en todo el mundo. [11]
Las plantas medicinales han llegado a adquirir una gran demanda en cuanto a terapias alternativas o complementarias en varias regiones del mundo. Las plantas con uso medicinal poseen como característica principal tener un alto contenido de sustancias o principios activos, con múltiples propiedades químicas, bioquímicas y organolépticas que permiten su mejor utilización con fines terapéuticos, plantas aromáticas o esencian, componentes del romero, su capacidad antioxidante, sus principales efectos son usados en la industria farmacéutica o terapéutica, en la industria alimentaria su uso es cada vez más abundante tal es el caso que uso toxicológico es parte de la industria. [12]
Se han registrado múltiples compuestos químicos presentes en el romero (R. officinalis L), los cuales han sido agrupados de forma general por distintos autores. Como son los ácidos fenólicos, flavonoides, aceite esencial, ácidos triterpénicos y alcoholes triterpénicos. [12]
Fig. 1. Romero
Fuente: [13]
Las ramas del romero presentan un aspecto seco propio de las zonas donde este crece, tal y como se puede observar en la Figura 1, es originario de la zona mediterránea, donde también se cultiva, los principales países productores son España, Marruecos y Túnez, pero también se la puede encontrar en Oceanía, Asia y en América del sur, Centroamérica y algunas partes del norte Americano, su recolección es por lo general en los meses de abril a julio su almacenamiento es en cajas de cartón o bolsas de papel. [8]
La distribución del romero (Rosmarinus officinalis L.) se localiza en el mediterráneo Sur de Europa y Norte de África, dichos lugares es donde el cultivo crece espontáneamente, esto se debe a los suelos arenosos y calcáreos, agroecológicamente las tierras bajas de clima cálido son las más propicias para desarrollar a esta planta, en la actualidad es cultivado en todo el mundo. [11]
En la siguiente imagen se muestra la distribución del romero a nivel global, cabe recalcar que se lo puede adquirir por lo general en la parte suroeste de Europa, norte de África, suroeste de Asia, así como en Latinoamérica. La introducción del romero en Latinoamérica se debe a los viajes realizados por los españoles en la época colonial, donde la utilizaban para fines medicinales en sustitución de los remedios aztecas.
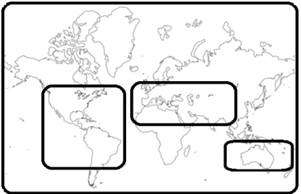
Fig. 2. Distribución Mundial del R. officinalis
Fuente: [12]
Existe una amplia cantidad de países donde se cultiva el romero, como productor se encuentran España, Marruecos y Túnez; aunque también se destaca en países con una producción relativamente moderada entre ellos están: Rusia, Inglaterra, Francia, Portugal, Túnez, China, Australia y Estados Unidos. El romero se cultiva dentro de los rangos de temperatura de 2ºC a 35ºC, fuera de este rango de temperatura el romero no posee un adecuado crecimiento.
1.3. Caracterización y morfología
Es una planta arbustiva, sus hojas son pequeñas y tienen forma de espigas con una coloración verde brillante. El romero es un arbusto de hasta dos metros de altura, florecen dos veces al año esta planta es muy resistente a los cambios de temperatura, su posición generalmente se mantiene erguida, sin embargo, en ocasiones se encuentra colapsada por otras plantas, el promedio de vida útil esta entre los 5 y 15 años. Su floración puede variar, pues mientras que algunos autores afirman que las flores pueden estar presentes en la planta durante todo el año, otros declaran que no hay floración durante los meses más calurosos del año. Parte del tallo crece recto con una característica aterciopelada y poseen numerosas glándulas esferoidales. [14]
Las hojas, tiene una estructura simple su tamaño regularmente es menor a 4-6 mm, sim embargo hay ramas que se diferencias a otras, características como en la parte exterior del borde de la hoja se observa que es aguda y entera, su oscilación es lineal y cóncava, sus márgenes son planos. En cuanto a la superficie foliar, las hojas jóvenes por lo general están sujetas al tallo sim embargo algunas con frecuencia lanoso. [14]

Fig. 3. Morfología del Romero
Fuente: [15]
1.4. Propiedades medicinales del Romero
Según [16], los antioxidantes son compuestos que retrasan la auto-oxidación de tal manera que proporcionan la inhibición o la formación de radicales libres. En la industria de la medicina es de gran importancia para la actividad antioxidante, datos del INEN, en Ecuador en el año 2015 se incrementó el uso de productos elaborados con esta planta hasta un 15% que, en años anteriores, esto se debe al potencial antioxidante que el romero posee.
En química los antioxidantes de origen natural provenientes de las plantas connotan en partes como el tallo, las hojas y las flores, en la actualidad son una alternativa convencional, esto se debe al alto contenido de compuestos fenólicos que pueden prevenir la propagación de reacciones de oxidación. [17]
Industrias como la farmacéutica, utilizan al romero en productos de salud y belleza, áreas como la cosmetología expresan que al incorporar infusiones o aceites de esta planta a un shampoo comercial, este fortalecerá las propiedades nutricionales que posee el romero, el objetivo de la mezcla es evitar la pérdida del cabello y dañar el cuero cabelludo. [18]
La “nanotecnología” terminología que proviene del latín (nanus: enano- Real Academia, 1895) se acuñó en 1974, fue expuesta por Norio Taniguchi de origen japonés en la (Universidad de Tokio, Japón) esto se dio para hacer o tener referencia acerca de cualquier tipo de tecnología que sea aplicada a escala atómica y molecular. En la actualidad esto ya se distinguen, de manera general, existiendo dos vías de desarrollo nanotecnológico, la primera revista que se creó en América latina en relación a los tópicos de comunicación informa que la vía de arriba abajo y la vía de abajo a arriba (top-down y bottom-up), una se refiere a “la versión dilatada que tiene como significado utilizar la tecnología que tenga relación con otros tipos de sustancias u objeto diminuto que posea un tamaño menor a 100 nanómetros (nm).”, en cuanto a la otra parte se basa en “proyectar, plasmar y construir máquinas que tengan la posibilidad de observar cada átomo y enlace químico si se encuentra precisamente especificado” (Storrs). La primera es la modalidad o versión ligera (light) y la segunda es una versión más compleja o también se la suele llamar como modalidad hard. [19]
Las nanociencias son un conjunto de disciplinas diversas que buscan comprender las leyes que gobiernan este universo diminuto. Las nanociencias tienen como propósito el estudio de las propiedades de la materia tanto de átomos como de moléculas (características térmicas, eléctricas, magnéticas, ópticas, químicas) esto quiere decir que las nanociencias contribuyen en gran magnitud a las investigaciones y estudios científicos: en mecatrónica, en ingeniería, en biología, en química tanto inorgánica como orgánica, en física en la mayoría de sus ramas: óptica, termodinámica, electrónica, hidráulica, etcétera. Las nanotecnologías, esto se refieren al conjunto de técnicas y procedimientos que permite la manipulación a nivel atómico y molecular de la materia, así como capacidad de configurar y cambiar voluntariamente sus características y desempeño (Royal Society: 2004).
Al ser combinadas estas tecnologías con los sistemas microelectro mecánicos (MEMS), el potencial de la computación y los conceptos de diseño estos se basan en sistemas biológicos, se construyen las condiciones para el desarrollo de objetos y materiales nanos que son capaces de responder a su ambiente. [19]
La nanotecnología es considerada como una ciencia “horizontal” esto se debe a que prácticamente tiene influencia, ya sea directa o indirectamente, sobre todos los sectores; es decir, tiene un enfoque interdisciplinario; de modo, que se proyecta que la nanotecnología podría ser la parte principal convergente dentro de la ciencia, la economía y la sociedad del futuro. Aquellos que promueven la nanotecnología, pronostican que esta no solo mejorará al mundo industrial, sino que lo reemplazará. El progreso nanotecnológico se ha considerado como un fenómeno, el cual se advierte por su constante incremento con relación a las patentes y entrevistas de la literatura científica, esto sin duda afectará de manera positiva la demanda de materiales nanoestructurados [20]
1.6. Nanotecnología en el Ecuador
Pese a que la nanotecnología a nivel mundial ha tenido un gran desarrollo y avance prolongado en esta área, en el Ecuador no se ha generado amplia información científica en esta rama, aunque en el país ya se están utilizando ciertos productos basados en la nanotecnología. Las investigaciones acerca de las nanopartículas son de mucha importancia, esto debido a que entre sus campos de aplicación están el medioambiente, exploración espacial, tecnologías de la comunicación e informática, sector energético, textil, construcción, y arquitectura, medicina, instrumentación, agricultura, ganadería, electrónica, cosmética, industria militar, automovilística, seguridad personal y vial, higiene y salud pública, deportes, espionaje, entre otras. [21]
Las nanopartículas de plata han generado un gran interés a lo largo de los años por sus propiedades fisicoquímicas a escala nanométrica muy especiales, que pueden ser aplicadas en distintas áreas como, por ejemplo, las nanopartículas de plata como agentes antibacteriales y antivirales; lo que las hace atractivas es precisamente su tamaño y forma. [21]
En la actualidad han aparecido distintos métodos para la síntesis de estos nanomateriales, teniendo un control tanto en la forma como en el tamaño de las (AgNPs), para ser empleadas en diversas aplicaciones, sin embargo, la mayoría de los métodos aplicativos para la síntesis de las nanopartículas son costosos y también agresivos con el medio ambiente, debido a esto se busca rutas sintéticas biológicas, o biosintéticas, que involucran organismos vivos totales como bacterias, hongos y plantas. Ecuador es considerado un país megadiverso en cuanto a recursos florísticos, es importante estudiar el potencial de plantas vegetales del Ecuador como agentes reductores y estabilizadores en los procesos de síntesis verde de nanopartículas [22].
Según las investigaciones de los autores antes mencionados se prevé, determinar la factibilidad del uso de una planta vegetal (romero) con propiedades antimicrobianas en este caso el romero, para sintetizar nanopartículas de plata, realizando varios procesos de síntesis teniendo en cuenta la concentración de extracto vegetal en el proceso, la temperatura y otras variables. Los resultados obtenidos en la síntesis se caracterizaron con las técnicas disponibles en el país [23].
Se
define así a los materiales que contienen partículas dentro del rango de la
nanoescala o escala nanométrica, es decir que vayan desde un nanómetro a 100
nm. El nanómetro (nm) al ser considerada en otra unidad (m) es equivalente a
una milmillonésima parte (![]() ).
Según la comisión europea en el 2011 se adoptó una recomendación sobre la
definición de nanomaterial, entendiéndose como tal un material natural,
accidental o fabricado que este contenga partículas, sueltas o formando un
agregado y en el que el 50 % o más de las partículas presentes en una o varias
dimensiones externas en el rango de tamaños comprendido entre (1 a 100)
nanómetros [24].
).
Según la comisión europea en el 2011 se adoptó una recomendación sobre la
definición de nanomaterial, entendiéndose como tal un material natural,
accidental o fabricado que este contenga partículas, sueltas o formando un
agregado y en el que el 50 % o más de las partículas presentes en una o varias
dimensiones externas en el rango de tamaños comprendido entre (1 a 100)
nanómetros [24].
Según Faraday y Turkevich (2009), propusieron uno de los mecanismos por el cual se da la formación de nanopartículas de plata. El mecanismo, está constituido por tres pasos fundamentales: nucleación, crecimiento y estabilización, como se puede apreciar en la figura 4.
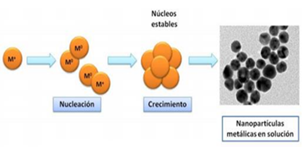
Fig. 4. Estructura de las Nanopartículas de Plata
Fuente: [25]
La nucleación inicia cuando se da una reducción de la sal metálica debido a la acción de un agente reductor que sea adecuado, generando átomos de metal con estado de oxidación cero, estos átomos metálicos con iones metálicos desencadenan la formación de un núcleo metálico al cual se le denomina semilla [25].
El crecimiento de los núcleos se da por difusión y debido a la transferencia de masa de los iones metálicos hacia la superficie de estos núcleos. Durante esta etapa, es necesario un control óptimo tanto de la temperatura como de la concentración debido a que estos tipos de parámetros influyen de forma significativa en mencionada etapa. La estabilización, depende del empleo de un agente de equilibrio, el cual actúa de manera que evita la aglomeración. El efecto es ocasionado por la repulsión entre partículas provocada por la doble capa eléctrica que se forma por los iones adsorbidos en la superficie de las nanopartículas [20].
1.9. Toxicidad de las nanopartículas de plata
En base al constante crecimiento con respecto a las aplicaciones que se les ha dado a las nanopartículas de plata, la exposición del cuerpo humano, así como también la liberación de estas al ambiente, se hace necesario realizar un análisis del potencial toxicológico que mencionadas nanopartículas puedan presentar.
A pesar de que la utilización de las (AgNPs) ya se ha reportado hace varios años, la evidencia de su toxicidad aún no está clara. Por lo que varios organismos acreditados, FDA (Food and Drug Administration) y la EPA (Enviromental Protection Agency), han aprobado el uso de estas nanopartículas en diversas industrias como textil, cosmética, alimentaria, entre otras. Entre estos organismos se encuentra también la Comisión Europea de Nanotecnología que establece que, la toxicidad de estas nanopartículas es muy baja por lo que en algunos de los productos actos para el consumo humano desprenden pequeñas cantidades de plata, por tanto, no ejercen consecuencias importantes para la salud [26].
Con respecto a la parte medioambiental se fundamenta que, el uso de la plata a escala nano constituye un porcentaje pequeño a diferencia de la cantidad de (Ag) total que se encuentra presente en el medio ambiente. Sin embargo, cabe resaltar que ciertas especies podrían absorber fácilmente esta plata especialmente los organismos acuáticos, pero que la probabilidad de ello es mínima [26].
Las investigaciones sobre las formas de interacción de estas nanopartículas con tejidos humanos y las principales rutas de exposición han demostrado resultados que reflejan a las nanopartículas de plata pueden presentar citotoxicidad por interacción con proteínas y enzimas a nivel intracelular.
Sin embargo, hasta ahora no se han reportado casos de efectos secundarios de productos que tengan relación con la utilización de las nanopartículas de plata, se mantienen las investigaciones para determinar si efectivamente las mencionadas nanopartículas son inocuas o no para el organismo, así como también para el medio ambiente [20]
2. Materiales y métodos
La recolección de datos es el resultado de una gran diversidad de técnicas y herramientas que son utilizadas para desarrollar la investigación, las cuales son la entrevista y la observación. El presente trabajo de investigación consta de un formato o prototipo investigativo basado en la aplicación de técnicas modernas de la investigación, modelos en los cuales pueden ser discriminatorios y cuestionables, son los que definirán y sistematizarán a las entrevistas a utilizar con este tipo de método se brindará un trabajo flexible en la recolección de datos:
En esta indagación, el fundamento primario compone textos científicos, tesis doctorales y los datos que se obtienen a partir de los ensayos experimentales efectuados en los laboratorios de la facultad de ingeniería química de la Universidad de Guayaquil, respecto a la síntesis de las nanopartículas de plata, y el efecto de estas nanopartículas sobre las bacterias E. coli, S. aureus y B. subtilis.
Desde otra perspectiva las fuentes de las indagaciones secundarias demuestran artículos de información reciente sobre la síntesis de diferentes tipos de nanomateriales, así como nanopartículas de oro y plata, métodos de modificación de superficies, microorganismos patógenos, y el efecto antimicrobiano que tendrán las nanopartículas.
La tabla 1, demuestra una lista de todos los equipos que se utilizan en la presente investigación así mismo también instrumentos muy importantes de laboratorio. Los cuales la mayoría están ubicados en la facultad de ingeniería química de la Universidad de Guayaquil. En el caso del Microscopio electrónico de barrido (SEM), este se ubica en el laboratorio de microscopia, localizado en instituto nacional de investigación en salud pública “Dr. Lepoldo Izquieta Perez”. Los análisis de terpenos y fenoles totales se los realizaron en “Laboratorio Analitico UBA”, mediante el cual se determinan la cantidad de terpenos y fenoles totales presentes en el extracto de romero.
Tabla 1.
Materiales y equipos utilizados
|
Equipos y herramientas de laboratorio |
Marca / Modelo |
Utilización |
|
Agitador magnético con calentamiento. |
Elicrom 4.8x22mm |
Realización del extracto de cilandro y en la síntesis de nanopartículas. |
|
Tirillas de pH |
Merck Millipore |
Control del pH del extracto y de las nanopartículas. |
|
Balanza analítica |
Elicrom |
Peso del sólido, nitrato de plata (AgNO3). |
|
Gradilla |
Fisher, Isolab, Bel-Ar scienceware |
Soporte para los tubos de ensayos. |
|
Equipo de Filtración |
|
Filtración del extracto |
|
Papel filtro Whatman N°1 |
Whatman |
Papel utilizado para retener los sólidos o grumos del extracto de romero |
|
Envases de ámbar |
Green
|
Envases para conservar las nanopartículas de plata y a su vez evitar que reciba la luz solar |
|
Vidrio Reloj |
Pyrex |
Utensilio de vidrio utilizado para pesar cantidades pequeñas de nitrato de plata |
|
Pipetas |
Pyrex |
Material volumétrico utilizado para medir las cantidades exactas de los reactivos en los ensayos fitoquímicos |
|
Estufa |
Memmert |
Secado de instrumentos y materiales de vidrio. |
|
Rejilla de Asbesto |
ASEMED |
Utilizada para mantener un equilibrio con respecto a la temperatura de una llama durante su calentamiento |
|
Hornilla eléctrica |
Corning PC-400D y Mtx |
Equipo calentador con el objetivo de elevar la temperatura para la realización del extracto de romero y síntesis de nanopartículas. |
|
Incubadora |
VWR |
Desarrollo y sostenimiento del cultivo de bacterias. |
|
Microscopio electrónico de barrido (SEM) |
JEOL JSM 5310 |
Determina la forma y el tamaño de las nanopartículas de plata |
|
Espectrofotómetro |
Genesys 10-uv |
Mide la absorbancia de una muestra en los espectros de luz ultravioleta y visible de 200 a 700 nm. |
|
Termómetro digital |
Multi-thermometer |
Controlador de temperatura en los diversos procesos |
|
Mortero |
|
Utensilio utilizado para machacar el romero. |
|
Refrigerador de laboratorio |
Labomersa & Mabe |
Utilizado para conservación a bajas temperaturas del extracto de romero, muestras de nanopartículas, agares preparados y utilizados, discos para inhibición. |
|
Cronómetro |
SmartWatch, Casio HS-3V-1 |
Controlador de tiempo para la síntesis de (AgNPs). |
· Para la preparación del extracto se siguió la metodología descrita por [27]. En este proceso se utilizaron las hojas de Rosmarinus officinalis (Romero), para la obtención de un extracto natural que favorezca el proceso de reducción del nitrato de plata y la formación de las nanopartículas, sin la necesidad de utilizar sustancias químicas contaminantes que podría generar sustancias tóxicas secundarias. El proceso de preparación del extracto comprende una serie de etapas nombradas a continuación:
· Recolección de la planta
· Selección y lavado de las hojas
· Reducción de tamaño utilizando un mortero
· Se hirvieron 100 g de hojas bien lavadas en un Beaker con 500 ml de agua destilada en un periodo de tiempo de 20 a 25 min hasta ebullición
· Se utilizó una plancha de calentamiento con agitador magnético para graduar la temperatura desde 50°C hasta 200°C manteniendo una agitación continua a 300 rpm.
· Se filtró el caldo producido, y posteriormente se agregaron 100g de hojas adicionales, hirviéndolo nuevamente bajo las mismas condiciones para concentrar la solución en función del contenido de Romero.
· Posteriormente se calentó el extracto concentrado para reducir su volumen por evaporación hasta 50 ml y así concentrar aún más el caldo.
· Por último, se filtró el extracto final, se dejó reposar a temperatura ambiente hasta que se enfríe y luego se almacenó en un recipiente de vidrio (matraz) esterilizado. Para conservar el extracto se mantuvo en refrigeración a una temperatura de 4°C.

Fig. 5. Extracto de hojas de romero con diferentes solventes
Para la determinación de los metabolitos secundarios se utilizó tres tipos de extracto cada uno con diferentes solventes; en agua destilada, en etanol y en agua acidulada; con la finalidad de utilizar el extracto que presente mayores compuestos y propiedades químicas para su determinado uso en la obtención de las nanopartículas.
2.2. Preparación del nitrato de plata acuoso (AgNO3)
Para realizar la respectiva preparación del nitrato de plata a una concentración de 1 [mM] se disuelve 0.034 gramos de AgNO3 en 200 ml de agua destilada en un recipiente de vidrio que se encontrará sellado hasta su respectivo uso. [28]
|
|
(1) |
|
|
|
|
(2) |
|
|
|
|
(3) |
|
|
|
|
(4) |
||
|
|
(5) |
|
|
2.3. Síntesis de nanopartículas de plata
Para la síntesis de nanopartículas de plata se siguió la metodología descrita por Camacho polo, estudio científico realizado en la Universidad de Cartagena, realizando varias modificaciones experimentales en las variables, de tal manera que se pueda obtener cuantitativamente una mejor eficacia en los resultados.
Se realizó la preparación de las nanopartículas de plata variando algunos factores como los días del extracto, el pH, y el volumen del extracto. En la siguiente tabla se describen las variables modificadas en la experimentación durante todo el proceso.
Variables modificadas en el proceso de elaboración de (AgNPs)
|
Extracto de romero |
||||||||||||||
|
1 (día) |
3 (días) |
|||||||||||||
|
Cantidad de extracto de romero (ml) |
Cantidad de extracto de romero (ml) |
|||||||||||||
|
5 |
10 |
20 |
30 |
40 |
5 |
10 |
20 |
30 |
40 |
|||||
|
pH |
pH |
|||||||||||||
|
8 |
9 |
10 |
8 |
9 |
10 |
|||||||||
Se inició utilizando el agente precursor nitrato de plata (AgNO3) químicamente puro y se preparó una disolución acuosa de un milimolar (mM).
Cabe recalcar que esa misma concentración del nitrato de plata se la utilizará en todo el proceso, variando el volumen del extracto de romero para comprobar mediante la experimentación cuál es la concentración más adecuada, dicho de esta manera. Se tomaron 5 ml de la solución de nitrato de plata de (1 mM) añadiéndole al extracto del romero a diferentes volúmenes de (5,10,20,30,40 ml), y titulando con hidróxido de sodio (NaOH) al 0.1N con la finalidad de ajustar el pH a básico. Para que se produzca esta reacción se la realiza con agitación constante a una temperatura de reacción (65°C) con variaciones en valores de pH (8,9 y 10).
Luego se almacenaron en frascos de ámbar de 30 y 100 ml de capacidad conservándolos a una temperatura de 4°C. El procedimiento descrito anteriormente se lo realizó variando el tiempo con relación al tiempo de elaboración del extracto en los días 1 y 3 dejándolo en reposo en refrigeración. Luego se observó en el espectrofotómetro en que día presentó una mejor absorbancia. A las muestras obtenidas se le realizaron un control de duración que fue de 1 a 7 días.
3. Resultados
Como resultado se obtuvo un extracto acuoso de las hojas de romero para la obtención de nanopartículas de plata; el extracto al ser caracterizado por ensayos cualitativos presentó cuatro de los metabolitos que se encuentran dentro de la composición química del romero, y mediante el análisis cuantitativo se obtuvieron excelentes resultados en el extracto acuoso, reportando presencia de fenoles y terpenos en un 24%. Esto quiere decir que en el extracto de las hojas de romero produce sus propios metabolitos secundarios con capacidad reductora, en este caso como agente reductor de la plata.
Análisis fitoquímico-contenidos en el extracto acuoso de las hojas de Rosmarinus officinalis
|
Ensayos fitoquímicos (Metabolitos secundarios) |
Extracto acuoso |
Extracto etanólico |
Extracto acidulado |
|
Saponinas |
Negativo |
Positivo |
Negativo |
|
Compuestos reductores(reactivo Fehling) |
Positivo |
Positivo |
Positivo |
|
Compuestos fenólicos |
Positivo |
Positivo |
Negativo |
|
Flavonoides |
Positivo |
Positivo |
Negativo |
|
Alcaloides: (ensayo de Dragendorff) |
(+++) (++) |
(+++) (+) |
(+) |
|
Resinas |
Negativo |
Negativo |
Negativo |
|
Terpenoides |
Positivo |
Positivo |
Positivo |
Como se observa en la tabla 3, no hubo presencia de saponinas debido a que no se presenció espumas en la muestra, ni de resinas por parte del extracto acuoso. Sin embargo, si hubo presencia de los compuestos esperados como lo son los compuestos fenólicos y los terpenoides seguido de azucares reductores, flavonoides y alcaloides.
Mediante el ensayo de los compuestos fenólicos se pudo comprobar la presencia de una coloración roja con un ligero color verde, cualitativamente esto quiere decir que hay presencia de ácidos fenólicos y se podría decir que pequeñas cantidades de taninos.
En la tabla 4 podemos observar cuantitativamente las cantidades de fenoles y terpenos contenidos en el extracto acuoso de romero, siendo estos los compuestos con mayores propiedades químicas.
Determinación cuantitativa de los principales metabolitos secundarios
|
Metabolito secundario |
Método |
Resultados |
Unidades |
|
Fenoles |
Singleton and Rosy |
24.0 |
% |
|
Terpenos |
2844.0 |
mg/kg |
Fuente: Laboratorios UBA
Elaborado por: (Arias & Palma, 2018)
3.2. Síntesis de nanopartículas de plata
En el proceso de síntesis de nanopartículas se observó que se produjo un cambio en la coloración de una tonalidad amarilla producto del mismo extracto a una coloración marrón oscuro. Diversos autores como [29], [30] y [31]; afirman que esta coloración es producto del crecimiento y desarrollo de las (AgNPs) cuando se utilizan solventes naturales de origen vegetal como extractos de cilantro, mático, sideroxylon capiri, vitis vinifera, nopal, sábila, etc.
Al finalizar el proceso las muestras de nanopartículas con pH 10, se las conservó en frascos de ámbar con aislamiento a la luz y conservándolas a temperaturas de 4°C. Las muestras de (AgNPs) se dejaron reposar de 1 a 3 días, donde se sembró en medios de cultivos en el día 0 y en el día 3, con el objetivo de comprobar el mejor efecto inhibitorio.

Fig. 6. Solución de (AgNPS) sintetizadas a partir de extracto de hojas de romero como agente reductor de la plata (Ag)
3.3. Caracterización de nanopartículas de plata (AgNPs)
Las nanopartículas fueron caracterizadas mediante el espectrofotómetro Genesys 10-uv.
Análisis de las (AgNPs) con diferentes volúmenes y pH 8 por Espectroscopía UV-VIS
|
Proporción en volumen |
Día |
Longitud de onda (𝝀) |
Absorbancia |
T (%) |
Factor de absorción (L/mol.cm) |
Concentración (mg/l) |
|
5-5 |
1 |
365 |
2.318 2.315 2.317 |
0.5 |
24.28 |
33.25 33.22 33.28 |
|
3 |
298 |
2.394 2.396 2.396 |
0.4 |
18.25 |
33.92 33.91 33.93 |
|
|
5-10 |
1 |
325 |
2.354 2.354 2.353 |
0.7 |
21.53 |
33.50 33.55 33.54 |
|
3 |
312 |
2.380 2.382 2.384 |
0.3 |
14.36 |
33.84 33.85 33.84 |
|
|
5-20 |
1 |
345 |
2.339 2.337 2.334 |
0.2 |
12.78 |
33.35 33.38 33.35 |
|
3 |
382 |
2.308 2.307 2.306 |
0.6 |
14.40 |
33.16 33.14 33.14 |
|
|
5-30 |
1 |
335 |
2.343 2.342 2.341 |
0.3 |
16.14 |
33.45 33.43 33.44 |
|
3 |
369 |
2.014 2.015 2.017 |
0.4 |
20.94 |
33.14 33.16 34.12 |
|
|
5-40 |
1 |
318 |
2.372 2.374 2.372 |
0.4 |
10.06 |
33.76 33.77 33.74 |
|
3 |
324 |
2.265 2.267 2.268 |
0.6 |
14.22 |
33.65 33.64 33.67 |
Al observar la tabla de datos tomados, en el espectrofotómetro se tienen valores que van desde 296 a 418 nm indicativo de que si existe presencia de nanopartículas, se descartó ciertos rangos que no son indicativos de una buena estabilidad en las NPs como son los rangos de 296 a 325 nm; esto debido a que la resonancia de plasmón superficial en la escala nanométrica del equipo espectrofotómetro absorbe la luz visible en los rangos de 400 a 800 nm y en relación al barrido electrónico se puede observar con respecto a los resultados los valores no sobrepasan de los 400 nm y en relación a la luz que transmitirán se proyectará tomando en cuenta que de acuerdo al valor de la longitud de onda se reflejará el color absorbido de la muestra, en esta tabla como se presentan rangos menores y si se observa en la tabla 5 no existe ninguna coloración que se refleje en estos rangos por tal motivo fueron descartados.
Análisis de las (AgNPs) con diferentes volúmenes y pH 9 por Espectroscopía UV-VIS
|
Proporción en volumen |
Día |
Longitud de onda (𝝀) |
Absorbancia |
T (%) |
Factor de absorción (L/mol.cm) |
Concentración (mg/l) |
|
5-5 |
1 |
402 |
2.403 2.405 2.405 |
0.5 |
16.10 |
34.02 34.05 34.04 |
|
3 |
390 |
2.435 2.432 2.430 |
0.3 |
14.12 |
34.30 34.32 34.31 |
|
|
5-10 |
1 |
396 |
2.412 2.414 2.414 |
0.4 |
18.02 |
34.15 34.16 34.19 |
|
3 |
342 |
2.478 2.476 2.478 |
0.5 |
12.11 |
34.87 34.87 34.88 |
|
|
5-20 |
1 |
376 |
2.419 2.420 2.422 |
0.8 |
19.24 |
34.78 34.79 34.81 |
|
3 |
369 |
2.424 2.422 2.423 |
0.6 |
17.05 |
34.81 34.84 34.84 |
|
|
5-30 |
1 |
395 |
2.416 2.416 2.418 |
0.4 |
13.72 |
34.21 34.23 34.24 |
|
3 |
382 |
2.438 2.438 2.440 |
0.3 |
11.23 |
34.52 34.54 34.55 |
|
|
5-40 |
1 |
388 |
2.426 2.426 2.428 |
0.6 |
17.99 |
34.48 34.46 34.46 |
|
3 |
309 |
2.396 2.396 2.398 |
0.4 |
14.42 |
34.90 34.92 34.94 |
Se observó que en la proporción 5-5 presentó una longitud de onda de 402 nm en el día 1, seguido de la proporción 5-10 con 396 nm en el mismo día; luego está 5-5 en el día 3. Estos valores lo que muestra es que en el día 1 presentan longitudes de onda mayores, aunque sus cantidades son muy cercanas. Esta tabla se descartó debido que en su mayoría presentaron valores con rangos bajos no obstante se tomó como referencia los dos valores que presentaron los mejores resultados en esta parte como lo son los de las proporciones de 5-5 y 5-10.
Análisis de las (AgNPs) con diferentes volúmenes y pH 10 por Espectroscopía UV-VIS
|
Proporción en volumen |
Día |
Longitud de onda (𝝀) |
Absorbancia |
T (%) |
Factor de absorción (L/mol.cm) |
Concentración (mg/l) |
|
5-5 |
1 |
418 |
2.328 2.326 2.329 |
0.4 |
16.98 |
34.21 34.27 34.25 |
|
3 |
405 |
2.362 2.363 2.362 |
0.2 |
14.12 |
34.72 34.75 34.76 |
|
|
5-10 |
1 |
409 |
2.374 2.373 2.376 |
0.4 |
12.32 |
34.61 34.67 34.65 |
|
3 |
412 |
2.312 2.317 2.318 |
0.5 |
14.54 |
34.50 34.52 34.52 |
|
|
5-20 |
1 |
404 |
2.368 2.367 2.367 |
0.4 |
16.38 |
34.78 34.77 34.77 |
|
3 |
399 |
2.416 2.417 2.418 |
0.3 |
15.03 |
34.84 34.84 34.83 |
|
|
5-30 |
1 |
401 |
2.392 2.395 2.394 |
0.3 |
12.14 |
34.80 34.81 34.80 |
|
3 |
410 |
2.364 2.363 2.361 |
0.4 |
14.74 |
34.66 34.66 34.67 |
|
|
5-40 |
1 |
389 |
2.425 2.427 2.423 |
0.4 |
13.37 |
34.96 34.97 34.95 |
|
3 |
400 |
2.396 2.398 2.397 |
0.5 |
15.02 |
34.90 34.92 34.94 |
En la tabla 7 se consideran que los datos en su mayoría son los mejores en comparación a los de la tabla 5 y 6, esto se debe a que las moléculas en pH básico se dispersan e interactúan de mejor manera lo que permite que al unirse la molécula de Ag con la del extracto se realice de una manera uniforme, de acuerdo a los resultados se obtienen valores muy cercanos es decir su variaciones son pequeñas, pero los mejores resultados se dieron en la proporción 5-5 con día 1 seguido de la proporción 5-10.
Se dice que cada planta contiene sus mismas propiedades químicas y que cada una puede reaccionar de diferente manera ya sea con rapidez o lentitud. En este caso el agente reductor del romero (ácido rosmarínico) reacciona con rapidez en el día 1 manteniendo sus valores en el rango hasta el día 3.
Entonces las nanopartículas obtenidas como resultado en pH 10 con proporción 5-5 en el día 1 presentaron una velocidad de reacción más elevada, teniendo el pico más alto con respecto a la gráfica y por consiguiente un valor en longitud de onda de 418 nm.
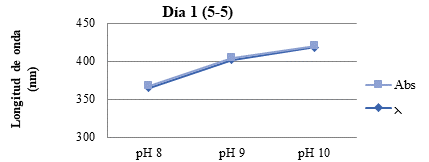
Fig. 7. Representación de los datos obtenidos en el equipo Espectrofotómetro Día 1 (5-5)
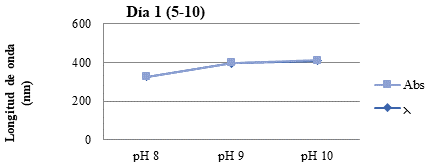
Fig. 8. Representación de los datos obtenidos en el equipo Espectrofotómetro Día 1 (5-10)
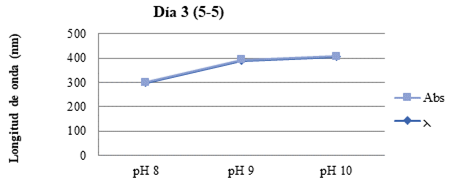
Fig. 9. Representación de los datos obtenidos en el equipo Espectrofotómetro Día 3 (5-5)
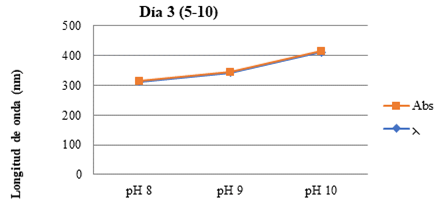
Fig. 10. Representación de los datos obtenidos en el equipo Espectrofotómetro Día 3 (5-10)
Medidas de los halos formados con respecto a las muestras analizadas
|
Muestras analizadas |
E. coli |
S. aureus |
B. subtilis |
|
Extracto
|
2.929 |
2.043 |
1.972 |
|
2.912 |
2.200 |
2.252 |
|
|
2.828 |
2.127 |
1.803 |
|
|
Promedio |
2.889 |
2.123 |
2.009 |
|
Solución de nitrato (AgNO3) |
1.803 |
1.296 |
1.093 |
|
1.418 |
1.313 |
9.31 |
|
|
1.430 |
1.319 |
1.133 |
|
|
Promedio |
1.550 |
1.309 |
1.052 |
|
Nanopartículas de plata (AgNPS)
|
3.255 |
2.082 |
2.329 |
|
3.218 |
2.269 |
2.341 |
|
|
3.159 |
2.197 |
2.168 |
|
|
Promedio |
3.211 |
2.182 |
2.279 |
Fuente: Laboratorio LAZO
Los resultados obtenidos demuestran que la solución de AgNO3 1mM y el extracto de romero poseen actividad antimicrobiana. Sin embargo, las nanopartículas de plata sintetizadas presentaron una mejor respuesta con respecto a la inhibición.
Las nanopartículas inhibieron tres tipos de bacterias presentando mayor sensibilidad en la bacteria E. coli esto se debe a que es una bacteria gram negativa, la cual cuenta con una triple capa en la pared celular una membrana conformada de fosfolípidos y lipopolisacáridos, una membrana citoplasmática y una fina capa de peptidoglicano a diferencia de las gram positivas, que posee una capa muy gruesa de peptidoglicano y su membrana citoplasmática. [32]
Por lo tanto, se puede anunciar que los mejores resultados se dieron en la bacteria gram negativa (E. coli), esto es debido a que poseen una capa más fina de peptidoglicano en comparación a las gram positivas (S. aureus y B. subtilis) las cuales tienen una capa mucho más gruesa lo que impide que las nanopartículas sintetizadas ingresen con facilidad en el interior de la membrana.
La inhibición provocada por las (AgNPs) presentaron halos que van desde los 2.1 cm a 3.2 cm el cual resultó ser el mayor diámetro.
Por tanto, se puede decir que las nanopartículas de plata sintetizadas con extracto de romero presentan actividad antimicrobiana en las bacterias E. coli, S. aureus y B. subtilis siendo más eficiente en la E. coli.
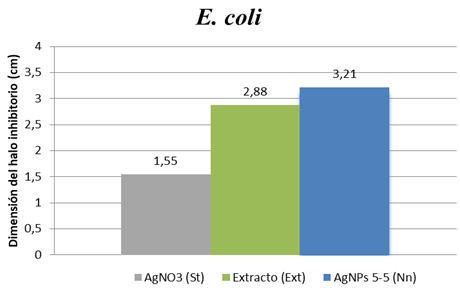
Fig. 11. Actividad antimicrobiana de las muestras utilizadas en la bacteria E. coli
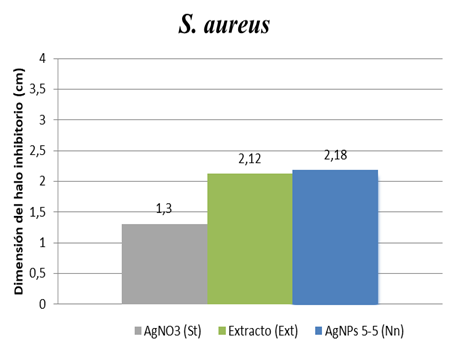
Fig. 12. Actividad antimicrobiana de las muestras utilizadas en la bacteria S. aureus
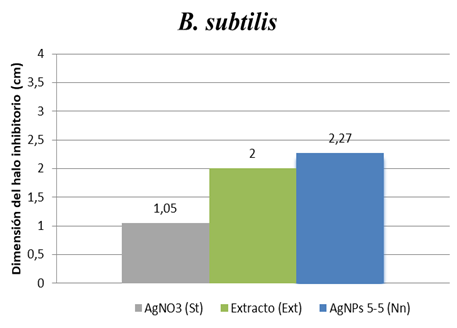
Fig. 13. Actividad antimicrobiana de las muestras utilizadas en la bacteria B. subtilis
4. Conclusiones
Se sintetizaron nanopartículas de plata utilizando el extracto de las hojas de romero, así como su estudio de la actividad antimicrobiana probadas en las cepas de E. coli, S. aureus y B. subtilis. Para lograr este tipo de acción fue necesario investigar las propiedades químicas reductoras del romero, así como cada mecanismo reductor de los iones plata, la interacción microbiológica que se puede generar.
En relación con los ensayos fitoquímicos realizados en el extracto acuoso de las hojas de romero, se puede decir que presenta los metabolitos secundarios más importantes entre ellos los ácidos fenólicos, flavonoides, terpenoides y compuestos reductores, al generar polifenoles esta planta es indicativa que puede desarrollar una excelente interacción con las moléculas del nitrato de Ag, aunque se estima que la reacción que se presenta se da con rapidez.
Los resultados obtenidos en la tabla 4 muestra el análisis realizado cuantitativamente por espectrofotometría, donde muestra que los resultados obtenidos en ácidos fenólicos son considerables puesto que el agente reductor se encuentra en la misma planta por naturaleza siendo factible para la sintetización de nanopartículas de plata.
Las (AgNPs) fueron caracterizadas por el espectrofotómetro uv-vis como se muestra en las tablas 5, 6 y 7; los mejores resultados se presentaron en la tabla de pH 10 en día 1 y con proporción v/v, esto es debido a que se detectó la mejor muestra en 418 nm representando el pico más alto con respecto a las gráficas; también gracias al equipo (SEM) se logró visualizar a las (AgNPs) obteniendo una morfología esférica con un tamaño de 10 nm, indicativo que se encuentra dentro del rango nanométrico, considerándose una excelente dimensión necesaria para inhibir en gran cantidad a los agentes patógenos.
Las (AgNPs) utilizadas en este trabajo generaron una acción antimicrobiana en los tres tipos de bacterias analizadas entre ellas la E. coli, S. aureus y B. subtilis; para probar la inhibición o qué tipo de bacteria presentó ser más sensible a las nanopartículas de plata sintetizadas, se utilizó el método (Bauer-Kirby); donde se observaron halos con tamaños desde 1 a 3 cm de diámetro, siendo muy eficiente; esto quiere decir que las (AgNPs) presentaron resultados con respuesta positiva a la acción antimicrobiana.
Como se indicó en el párrafo anterior, que en los tres tipos de bacterias presentó inhibición, sin embargo, los halos con mayor magnitud se dieron en la bacteria gram negativa (E. coli) debido a que posee una capa más fina en su membrana en comparación a las gram positivas. La (E. coli) fue la que presentó una mayor sensibilidad frente a las nanopartículas de plata sintetizadas (AgNPs), seguido de las gram positivas (S. aureus y B. subtilis). Cabe recalcar que los mejores resultados de acuerdo con las siembras realizas, fueron en tiempo cero, manteniendo una mayor estabilidad e interacción las bacterias.
Se comprobó el efecto antimicrobiano en manzanas rojas, donde se utilizó las nanopartículas y la cera de abejas como conservante, este compuesto retardó el proceso de maduración, mantuvo su peso final con respecto al inicial y lo más importante que impidió que cualquier tipo de microorganismo ingresara en el interior de la fruta. Por lo tanto, se puede concluir que este trabajo es muy eficiente para conservar frutas de manera natural, sin variar sus propiedades organolépticas.
Referencias
|
[1] |
T. . P. Purca Peña , «Efectividad antibacteriana "in vitro" del extracto de Rosmarinus officinalis (romero) sobre flora salival,» Universidad Nacional Mayor de San Marcos , pp. http://docs.bvsalud.org/biblioref/2018/03/880127/efectividad-antibacteriana-in-vitro-del-extracto-etanolico-de-r_mnpx4pV.pdf, 2013. |
|
[2] |
C. . I. Beristain Guevara y L. A. Pascual Pineda, «Diseño y funcionalidad en sistemas in vivo de nanocápsulas liquidas de aceite de romero (Rosmarinus officinalis L.),» Universidad veracruzana, pp. https://www.uv.mx/mca/files/2018/01/I-en-A.-Jesus-Alberto-Briones-Concha.pdf, 2017. |
|
[3] |
H. Castaño, «Actividad bactericida del extracto etanólico y del aceite esencial de hojas de Rosmarinus officinalis L. sobre algunas bacterias de interés alimentario,» Vitae, revista de la Facultad de Química Farmacéutica, p. http://www.redalyc.org/pdf/1698/169815396006.pdf, 2010. |
|
[4] |
C. Flores, «Nanopartículas de plata con potenciales aplicaciones en materiales implantables: síntesis, caracterización fisicoquímica y actividad bactericida,» Universidad Nacional de la Plata, pp. http://sedici.unlp.edu.ar/bitstream/handle/10915/34946/Documento_completo.%20Flores%20-%20Area%20Qu%C3%ADmica.pdf?sequence=1, 2014. |
|
[5] |
M. Sánchez Moreno, «Nanopartículas de plata: Preparación, caracterización y propiedades con aplicación en inocuidad de los alimentos,» Universidad Nacional de Educación a distancia, pp. http://e-spacio.uned.es/fez/eserv/bibliuned:master-Ciencias-CyTQ-Msanchez/Sanchez_Moreno_Minerva_TFM.pdf, 2017. |
|
[6] |
A. T. Madrid Sani, «"Síntesis y caracterización de nanopartículas de plata a partir de varios extractos pigmentados de dos plantas para su aplicación en celdas solares híbridas",» ESPE, pp. https://repositorio.espe.edu.ec/bitstream/21000/12797/1/T-ESPE-053784.pdf, 2017. |
|
[7] |
. A. R. Navarro Cruz y R. Avila Sosa, «Romero (Rosmarinus officinalis L.),» Benemérita Universidad Autónoma de Puebla, p. http://www.umar.mx/revistas/43/0430103.pdf, 2011. |
|
[8] |
J. A. Briones Concha, «Diseño y funcionalidad en sistemas in vivo de nanocápsulas liquidas de aceite de romero (Rosmarinus officinalis L.),» 13 Diciembre 2017. [En línea]. Available: https://www.uv.mx/mca/files/2018/01/I-en-A.-Jesus-Alberto-Briones-Concha.pdf. |
|
[9] |
N. Carrasco, Romero origen y ditribución, Bogota: TYIE, 2009. |
|
[10] |
N. P. González Villalva, «“Extracción y caracterización de los antioxidantes secundarios del romero (Rosmarinus officinalis L.),» 13 Septiembre 2013. [En línea]. Available: http://repositorio.uta.edu.ec/bitstream/123456789/6565/1/AL%20521.pdf. |
|
[11] |
L. A. Perez, «Romero distribucion latinoamericana,» Pussy , pp. 11 - 14, 2011. |
|
[12] |
M. Valdés Flores y L. Quiroz Charles, «Universidad Autónoma de Coahuila Coordinación Unidad Saltillo,» On- Ciencia , p. http://www.posgradoeinvestigacion.uadec.mx/Documentos/Libros/2017onciencia.pdf, 2017. |
|
[13] |
M. Sanchez, «Jardineria ON,» 06 Febrero 2018. [En línea]. Available: https://www.jardineriaon.com/como-reproducir-el-romero.html. |
|
[14] |
V. Lax Vivancos, «Estudio de la Variabilidad Química, Propiedades Antioxidantes y Biocidas de Poblaciones Espontáneas de Rosmarinus Officinalis L. en la Región de Murcia,» Universidad de Murcia , p. https://www.tdx.cat/bitstream/handle/10803/284820/TVLV.pdf, 2014. |
|
[15] |
L. A. Larrain, «Morfologia del Romero,» Loor, Cali, 2016. |
|
[16] |
Y. L. Pardo y R. Ordoñez, «Cuantificación de hierro, calcio y fósforo en procesos térmicos aplicados al borojó ( Borojoa patinoi Cuatrec),» Idesia, pp. 3 - 4 , 2018. |
|
[17] |
G. Fonnegra, «Plantas medicinales aprobadas en Colombia,» de Plantas medicinales aprobadas en Colombia , Antioquia, Universidad de Antioquia, 2007, p. 222. |
|
[18] |
M. Arango Mejía, «Plantas medicinales: botanica de interest medico,» de Botanica de interest medico, Buenos Aires, Poest, 2006, p. 283. |
|
[19] |
A. Guzmán Chávez y A. Toledo Patiño, «Las nanotecnologías,» RYP, p. http://www.razonypalabra.org.mx/N/n68/6AlenkaToledo.pdf, 2009. |
|
[20] |
M. A. Salguero, «Síntesis y caracterización de nanopartículas de plata usando como reductores extractos de menta (Origanum vulgare) y cilantro (Coriandrum sativum) y como funcionalizante el látex de sangre de drago (Croton lechleri),» Pontificia Universidad Católica del Ecuador, p. http://repositorio.puce.edu.ec/bitstream/handle/22000/12552/MARCELO%20SALGUERO%20S..pdf?sequence=1&isAllowed=y, 2016. |
|
[21] |
A. I. Torres, «Síntesis verde y caracterización de nanopartículas de oro y plata mediante el uso de algunas plantas endémicas del Ecuador,» Escuela Politécnica Nacional, pp. file:///C:/Users/ANNELIESE%20P/Downloads/CD-7681%20(1).pdf, Noviembre 2016. |
|
[22] |
J. Echeverry-Chica, A. Naranjo-Díaz y P. Araque-Marín, «Nanopartículas de plata funcionalizadas in situ con D-limoneno: efecto en la actividad antibacteriana,» Revista ION, vol. 33, nº 1, 2020. |
|
[23] |
S. Estrada Orozco, «Determinación de la actividad antibacteriana in vitro de los extractos de romero,» Escuela Superior Politécnica de Chimborazo, p. http://dspace.espoch.edu.ec/bitstream/123456789/699/1/56T00229.pdf, 2010. |
|
[24] |
INSHT, «Seguridad y salud en el trabajo con nanomateriales,» Nanomateriales, p. http://www.insht.es/InshtWeb/Contenidos/Documentacion/FICHAS%20DE%20PUBLICACIONES/EN%20CATALOGO/Higiene/2015%20Seguridad%20y%20salud%20en%20el%20trabajo%20con%20nanomateriales/SST%20con%20nanomateriales.pdf, 2015. |
|
[25] |
C. Flores y C. Vericat, «Nanopartículas de plata con potenciales aplicaciones en materiales implantables: síntesis, caracterización fisicoquímica y actividad bactericida,» Universidad Nacional De La Plata, La Plata, 2014. |
|
[26] |
M. Sánchez, «Nanopartículas de plata: Preparación, caracterización y propiedades con aplicación en inocuidad de los alimentos.,» Departamento de química inorgánica y química técnica, pp. http://e-spacio.uned.es/fez/eserv/bibliuned:master-Ciencias-CyTQ-Msanchez/Sanchez_Moreno_Minerva_TFM.pdf, Octubre 2017. |
|
[27] |
J. Camacho Polo, «Síntesis de nanopartículas de plata y modificación con pulpa de papel para aplicación antimicrobial,» Universidad de Cartagena, p. 12, 2013. |
|
[28] |
C. Sánchez, «Sintesis Nanopartículas,» Research Gate, 2016. |
|
[29] |
A. Borja y I. López, «Obtención y caracterización de nanopartículas de plata soportadas en fibra de algodón,» SCIELO, pp. http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1665-35212013000300001, 2013. |
|
[30] |
M. Salguero, «Síntesis y caracterización de nanopartículas de plata usando como reductores extractos de menta (Origanum vulgare) y cilantro (Coriandrum sativum), y como funcionalizante el látex de sangre de drago (Croton lechleri),» Pontificia Universidad Católica del Ecuador, p. http://repositorio.puce.edu.ec/bitstream/handle/22000/12552/MARCELO%20SALGUERO%20S..pdf?sequence=1, 2016. |
|
[31] |
M. Hernández, «“Síntesis de nanopartículas de plata biológicamente asistida con Opuntia sp, y su incorporación en membranas poliméricas nanofibrosas”,» Centro de Investigación en Química Aplicada, p. https://ciqa.repositorioinstitucional.mx/jspui/bitstream/1025/64/1/Tesis%20de%20maestria%20Marco%20Polo%20Hernadez.pdf, 2013. |
|
[32] |
L. Monroy, «Uso de Nanopartículas de plata en el control de microorganismos patógenos presentes en alimentos,» Limentech Ciencia y Tecnología Alimentaria, p. http://www.unipamplona.edu.co/unipamplona/portalIG/home_206/recursos/general/02032016/alimentech.pdf, 2015. |