RESUMEN
Antecedentes:
La obesidad asociada a diabetes es una afección
potencialmente mortal. Actualmente, la cirugía representa una opción
terapéutica eficaz y duradera para tratarla, siendo el bypass gástrico el
procedimiento estándar, demostrando un efecto
significativo en la pérdida ponderal y en la resolución de diabetes. Objetivo:
Comparar resultados que demuestren la
eficacia de cada técnica del bypass gástrico en el hospital ¨Abel Gílbert
Pontón¨, enfocando los beneficios, complicaciones y evolución de cada grupo. Metodología:
Estudio observacional, retrospectivo, analítico, comparativo y longitudinal,
realizado en el Hospital Abel Gílbert Pontón, durante el período 2015-2019. La
población estuvo conformada por pacientes con diagnóstico de obesidad y
diabetes mellitus tipo 2 sometidos a bypass gástrico. Resultados: Se
analizaron 76 pacientes, de los cuales 46 se sometieron a BAGUA y 30 a BGYR. Al
comparar la pérdida de peso, no se observó diferencia significativa en ninguno
de los tiempos de seguimiento (3, 6 y 12 meses), pero se evidenció diferencias
significativas sobre el tiempo quirúrgico, estancia hospitalaria, e ingreso a
UCI, a favor de BAGUA. Se evidenció mayor remisión de diabetes mellitus para el
BAGUA. El BGYR estuvo más relacionado con complicaciones (sangrado, fuga
anastomótica y reoperación). No hubo diferencia en la presencia de reflujo
biliar gastroesofágico. Falleció un paciente (1,32%), el cual había sido
intervenido mediante BGYR. Conclusiones: BAGUA es un procedimiento eficaz
para la pérdida de peso, con iguales o mejores beneficios que BGYR, y posee
mayor efectividad en remisión de diabetes mellitus; además, es más seguro, con
menor morbilidad y menos reoperación.
PALABRAS
CLAVE: Obesidad, Diabetes mellitus tipo 2, Bypass
Gástrico, BAGUA,
Y de Roux (BGYR)
ABSTRACT
Background:
Obesity associated with diabetes is a life-threatening condition. Currently,
surgery represents an effective and long-lasting therapeutic option to treat
it, with gastric bypass being the standard procedure, demonstrating a
significant effect on weight loss and resolution of diabetes. Objective:
To compare results that demonstrate the efficacy of each gastric bypass
technique in the ¨Abel Gílbert Pontón¨ hospital, focusing on the benefits,
complications, and evolution of each group. Methodology: Observational
study, retrospective, analytical, comparative, and longitudinal, carried out at
the Abel Gílbert Pontón Hospital, during the period 2015-2019. The population
consisted of patients diagnosed with obesity and type 2 diabetes mellitus who
underwent gastric bypass. Results: 76 patients were analyzed, of which
46 underwent BAGUA and 30 under RYGB. When comparing weight loss, no
significant difference was noted in any of the follow-up times (3, 6, and 12
months), but significant differences were observed regarding surgical time,
hospital stay, and ICU admission, in favor of BAGUA. Greater remission of
diabetes mellitus was evidenced for BAGUA. RYGB was more related to
complications (bleeding, anastomotic leak and reoperation). There was no
difference in the presence of gastroesophageal bile reflux. One patient died
(1.32%), who had undergone RYGB. Conclusions: BAGUA is an effective
procedure for weight loss, with equal or better benefits than RYGB, and has
greater effectiveness in remission of diabetes mellitus; Furthermore, it is
safer, with less morbidity and less reoperation.
KEY
WORDS: Obesity, Type 2 Diabetes mellitus, Gastric
Bypass, BAGUA.
INTRODUCCIÓN
La
Obesidad es una enfermedad relacionada con la reducción de la esperanza de
vida, ya que aumenta el riesgo de morbilidad y mortalidad de quienes la
padecen. Considerada como una epidemia, la Obesidad ha demostrado en múltiples
investigaciones una estrecha relación entre ésta y la diabetes mellitus (DM),
de este modo, el aumento del Índice de Masa Corporal (IMC) y la obesidad
abdominal se asocia con un mayor riesgo de sufrir diabetes mellitus tipo 2,
convirtiéndose en un factor predictivo fiable de sufrir esta enfermedad.(1)
La
diabetes mellitus tipo 2 inducida por la obesidad está aumentando a nivel
global, correlacionándose con un aumento comparativamente pronunciado en la
prevalencia de la obesidad, la cual se la consideraba antes un problema de los
países desarrollados. En la actualidad, ambos trastornos incrementan de manera
considerable en los países en vías de desarrollo, repercutiendo de manera
significativa a los sistemas de salud. A pesar de los cambios en el estilo de
vida, dieta y ejercicio, la prevalencia de estas patologías asociadas sigue en
crecimiento, siendo en muchos casos de difícil manejo y de adaptación a su
tratamiento, por consiguiente, sus complicaciones aumentan la morbimortalidad
de quienes las padecen.(1)
Figure 1 Obesidad
mórbida intervenido de cirugía metabólica (BAGUA)
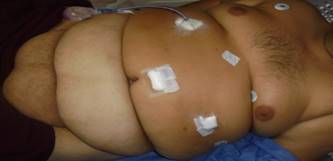
Fuente: Elaboración propia
En
ese sentido muchos pacientes son candidatos para recibir tratamiento quirúrgico
con el objetivo de lograr una disminución satisfactoria y sostenida de su masa
ponderal y control metabólico adecuado. La cirugía de la Obesidad ha sido
reconocida a través de la historia con el desarrollo de técnicas quirúrgicas
que inicialmente se asociaban a múltiples complicaciones, no obstante, se
fueron perfeccionando dichas técnicas hasta llegar a considerar a la cirugía
metabólica como la terapéutica más efectiva, siendo cada día más útil en el
manejo de la obesidad y control de sus comorbilidades a largo plazo.(2)
De
acuerdo a la Federación Internacional de Cirugía de la Obesidad y Trastornos
Metabólicos (IFSO), quien describe el patrón de la práctica quirúrgica
metabólica actual, el bypass gástrico representa el 39% de todos los procedimientos
quirúrgicos bariátricos que se realizan a nivel mundial, de acuerdo al 5to
registro global desarrollado en 2019.(3)
Según
con las estadísticas de la Sociedad Americana de Cirugía Bariátrica y
Metabólica, conforme va aumentando el grado de experiencia en el tema, el
bypass gástrico representa a más del 80% de todas las cirugías malabsortivas
mixtas correspondientes a su tipo. La mayoría de los pacientes diabéticos
sometidos a bypass gástrico logran conseguir niveles normales de glicemia sin
tratamiento con drogas hipoglicemiantes. (4)
La
cirugía Bariátrica para el tratamiento de la obesidad se creó en el año 1954
mediante la derivación yeyunoileal o bypass intestinal, con la intención principal
de disminuir la masa ponderal en aquellos pacientes refractarios al tratamiento
médico. Kremen y Linner en Minnesota desarrollaron esta cirugía con el objetivo
de reducir la superficie de absorción intestinal, iniciando así los
procedimientos quirúrgicos malabsortivos, consiguiendo que los pacientes
disminuyeran satisfactoriamente su peso e incluso lo mantuvieran por largo
tiempo. sin embargo, a largo plazo fueron apareciendo complicaciones de problemas
malabsortivos y síndrome de intestino corto, que hicieron que la derivación
yeyuno-ileal no fuera un procedimiento admisible.(5)
En
la cirugía de pérdida de peso, el concepto de bypass gástrico de una
anastomosis fue introducida por primera vez por Mason en 1967, en donde la
bolsa gástrica era más ancha y corta, de forma horizontal, exponiendo a la
mucosa esofágica al reflujo biliar proveniente del asa yeyunal, debido a
aquello, este concepto de derivación fue ágilmente abandonado.(5)
Durante
la década de los setenta, Scopinaro en Italia creó la segunda generación de
técnicas de mala absorción, configurando así, el primer procedimiento
bariátrico combinado, la ¨derivación biliopancreática¨, una modificación de la
derivación yeyuno-ileal que consistía en un reservorio gástrico horizontal de
200-250 ml asociado a una gastrectomía distal con cierre del muñón duodenal y
una gastroyeyuno anastomosis en Y de Roux con 250 cm de asa alimentaria,
encontrando como complicaciones importantes a lo largo del tiempo: anemia,
déficit de minerales (hierro y calcio), vitaminas liposolubles y proteínas,
además de reportarse series de síndrome postgastrectomía (úlceras marginales y
dumping).(6)
En
1994, el Dr. Wittgrove fue el primero en describir el bypass gástrico en ¨Y de
Roux¨ (BGYR) por vía laparoscópica, pero poco tiempo después en 1997, Rutledge
en Estados Unidos, instauró una versión distinta de bypass gástrico de una sola
anastomosis, con una modificación simplificada del
tradicional bypass gástrico en ¨Y de Roux¨ (BGYR), fue
denominado mini bypass gástrico (MBG) porque el
procedimiento inicialmente fue descrito a través de una ¨mini laparotomía¨. El
mini bypass gástrico consistía en una manga larga proyectada sobre la curvatura
menor del estómago, donde luego se construye una anastomosis antecólica de 3 a
5 cm de ancho entre la bolsa gástrica y el yeyuno, hacia alrededor de 120 a 180
cm distales al ligamento de Treitz. En los súper obesos, la distancia al
ligamento de Treitz sería de unos 250 cm.(5)(7)
En
2002, Carbajo y Caballero en España propusieron una variación de la técnica
para prevenir el reflujo biliar gastroesofágico, la cual llamaron en español
¨bypass gástrico de una anastomosis¨ (BAGUA). Según esta técnica, se realiza
una sola anastomosis laterolateral entre el asa del yeyuno y la bolsa gástrica,
y la distancia al ligamento de Treitz promedio es entre 250 y 350 cm. En 2013,
la confusión creada por los diferentes nombres a lo largo del tiempo llevó a un
grupo de cirujanos de la Federación Internacional de Cirugía de la Obesidad y
trastornos metabólicos (IFSO) a usar el nombre de mini bypass gástrico de una
sola anastomosis (MGB-OAGB) para definir esta cirugía.(8)
En
el 2017, Cohen et al. realizaron un metaanálisis que fortaleció el concepto de
incorporar la cirugía metabólica, particularmente el bypass gástrico en ¨Y de
Roux¨ (BGYR), al tratamiento médico, siendo la mejor opción para el manejo de
la DM2 no controlada en pacientes Obesos. Los mecanismos propuestos incluyen la
reducción de la ingesta calórica, absorción reducida de nutrientes y cambios en
las hormonas incretinas, como el péptido similar a glucagón 1 (GLP-1).(9)
Comparar la eficacia
del bypass gástrico laparoscópico de una sola anastomosis (BAGUA) frente al
bypass gástrico en ¨Y de Roux¨ en pacientes con Obesidad y Diabetes mellitus
tipo 2, en el hospital “Abel Gilbert Pontón”, periodo 2015-2019.
BYPASS GÁSTRICO EN Y DE
ROUX:
Actualmente,
el bypass gástrico en Y de Roux (BGYR) es la principal técnica metabólica mixta
de elección en muchos centros de cirugía metabólica, con respecto a pacientes
con obesidad mórbida y trastornos metabólicos, o como procedimiento de rescate
después de una cirugía bariátrica fallida. Esta técnica quirúrgica tiene como
objetivo realizar un reservorio gástrico de 25 a 30cc. de capacidad en la parte
superior del estómago, cerca de la unión esofagogástrica; y crear una
gastroyeyunoanastomosis en Y de Roux a una distancia variable según el grado de
obesidad.(17)
Figure
2 Esquema del
bypass gástrico en Y de Roux (BGYR)
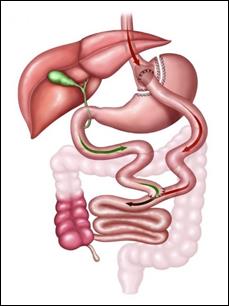
Si bien
hay muchas variaciones sobre el tema, existen ciertas características definidas
y componentes de la técnica quirúrgica que son comunes a todos los
procedimientos que llevan este nombre, los cuales se describen continuación.
Creación
de la rama de Roux: Porción Intestinal.
A
través de una técnica estándar laparoscópica de cinco puertos, ésta
parte de la cirugía se inicia mediante la identificación del ligamento de
Treitz, una vez identificado, se divide el yeyuno proximal entre 30 y 50 cm
distal al ligamento. Cuanto más corta sea la distancia, mejor se produce la
absorción de hierro y calcio. (18)
El yeyuno se separa utilizando uno o dos disparos de la
grapadora tipo GIA utilizando una carga de cartucho blanco, la segunda carga de
grapas a menudo puede extenderse en el mesenterio, esto es útil para comenzar
el aumento de la movilidad de la rama de Roux, sin embargo, la división del
mesenterio debe continuarse en sentido directamente hacia abajo, de igual modo
separando el mesenterio entre los dos segmentos del intestino dividido.(18)
Los extremos del yeyuno se evalúan por viabilidad,
cualquier porción isquémica se reseca de nuevo. En el extremo de la rama de
Roux, se sutura a manera de guía, un drenaje de Penrose de 0,25 pulgadas, el
final de la rama de Roux siempre debe estar sostenido por una pinza, hasta que
se una al drenaje guía, esto se hace para evitar cualquier posibilidad de
confundir la rama de Roux con el extremo biliopancreático.(18)
La rama de Roux se mide ahora en longitud, generalmente
se realiza longitudes de la rama de Roux, de aproximadamente 100 cm para los
pacientes con un IMC de 40 a 50, 125 a 130 cm para los pacientes con un IMC de
50 a 55 y 150 cm para un IMC superior a 55. Una vez que se mide la longitud
apropiada del extremo de Roux, ese punto se sutura al extremo biliopancreático
con una sola sutura en el lado antimesentérico de la extremidad
biliopancreática aproximadamente 6 cm proximal a su final.(18)
El bisturí armónico se utiliza ahora para crear una
enterotomía, 1 cm distal a la sutura que sostiene los dos segmentos del
intestino, junto a los lados antimesentéricos de cada segmento intestinal.
Estás enterotomías deben ser adyacentes entre sí, para luego colocar las patas
de 45 mm de la grapadora GIA de carga blanca en cada enterotomía, insertándola
completamente en la luz intestinal, es cerrada y activada. Una segunda carga
blanca se coloca en el sitio de la enterotomía, la grapadora se coloca
completamente en la luz intestinal que casi siempre es lo suficientemente larga
para acomodar la pata superior en el segmento corto de la extremidad
biliopancreática distal, la grapadora es cerrada y activada. La enterotomía
suturada ahora es cerrada. Por último, el defecto mesentérico de la
entero-enterostomía, se cierra con una sutura permanente.(18)
Pasando la extremidad de Roux:
Varios Autores prefieren realizar una vía retrocólica y
retrogástrica, para la rama de Roux, ya que permite pasar la rama a través de
la distancia más corta hasta el estómago proximal, minimizando el riesgo de
tensión de la anastomosis. Otros autores proponen un pase de la rama de Roux
antecólica, argumentando que este método es más rápido y tiene poco riesgo de
problemas en la anastomosis debido la tensión.(18)
El mesenterio del colon transverso justo a la izquierda
del ligamento de Treitz es levantado y estirado de forma que presente una
superficie plana sólida, el área justo a la izquierda y por encima del
ligamento de Treitz, usualmente sirve como lugar seguro para crear una abertura
con el bisturí ultrasónico. Se hace una abertura longitudinal de varios
centímetros de diámetro y el mesenterio es separado cuidadosamente con el
bisturí ultrasónico.(18)
Una vez que se hace la abertura, el estómago suele ser
visible fácilmente y puede ser captado dirigiéndolo hacia la apertura del
mesenterio. La ampliación de la apertura mesentérica permite suficiente espacio
para pasar la rama de Roux, en el espacio retrogástrico, esto se facilita
mediante la localización del dren de penrose guía y se lo pasa a través de
espacio, seguido por las primeras 2 o 3 pulgadas de la rama de Roux. Se debe
tener cuidado de que el mesenterio de la rama de Roux no esté torcido a medida
que se pasa a través del mesenterio del colon transverso.(18)
Creación de
la bolsa gástrica proximal:
La bolsa gástrica proximal está mejor construida a partir
de la curvatura menor del estómago, con sólo una cantidad mínima de fondo
gástrico incluido. Con el fin de exponer mejor al estómago, se coloca al
paciente en posición inversa de trendelemburg relativamente empinado. El
bisturí ultrasónico se utiliza entonces para crear una abertura en el
mesenterio de la curvatura menor adyacente al estómago. Más a menudo, se crea
la bolsa a partir de varios centímetros por encima de la incisura angularis,
una vez que se hace la abertura, la grapadora GIA de carga azul es activa
directamente a través del estómago, creando un corte dividiendo el estómago,
desde el lado de la curvatura menor.(18)
El cirujano debe hacer doble confirmación con el
anestesiólogo ante cualquier sonda nasogástrica, u otros tubos que podrían
estar en el lumen del estómago, estas deben ser retiradas antes de activar la
grapadora. Se ha encontrado que el paso a seguir para guiar el tamaño de la
bolsa es que el anestesiólogo pasé una sonda calibradora de 32 French de
diámetro. Esta sonda calibradora se coloca entonces a lo largo de la curvatura
menor del estómago y sirve como guía para crear el tamaño de la bolsa.(18)
La grapadora GIA es activada varias veces adyacente al
lado del tubo hasta que la parte superior del estómago se alcance en la zona
del ángulo de His, debe crearse una abertura a través del mesenterio por debajo
del borde de la parte superior del fondo para facilitar la activación final de
la grapadora, permitiendo la separación completa del estómago y por lo tanto la
separación completa de la bolsa gástrica proximal del estómago distal.(18)
Creación de
la Gastroyeyunostomía:
Una vez creada la bolsa gástrica el drenaje de penrose es
normalmente visible detrás de la parte baja del estómago. Una vez que el
drenaje de penrose se ha localizado, se utiliza para tirar suavemente la rama
de Roux hasta pasar la parte inferior del estómago. El extremo proximal de la
rama de Roux se coloca adyacente al extremo más inferior de la bolsa gástrica
proximal. Una vez que los dos órganos están alineados, se utiliza una sutura
continua para conectar el lado de la rama de Roux con la línea de grapas de la
bolsa gástrica proximal.(18)
Se crea una gastrotomía en la bolsa del estómago distal,
cerca de 1 cm del extremo. Se realiza una enterotomía adyacente en la rama de
Roux utilizando el bisturí ultrasónico para ambos. Se le pide al anestesiólogo
que retire la sonda calibradora 6 a 8 cm, con el fin de evitar graparla, la
confirmación visual de esto es obligatoria, la carga azul de la grapadora GIA
se inserta ahora en los dos lúmenes, un extremo en cada uno. Se alinea con la
dirección natural de los órganos, y la grapadora es activada.(18)
La enterotomía remanente se cierra, utilizando un plano
de sutura contínua absorbible, este cierre de la enterotomía se refuerza luego
con un plano exterior de sutura absorbible, después se avanza la sonda
calibradora, justo al otro lado de la anastomosis, a continuación, probamos que
no haya fugas, forzando la inyección de azul de metileno por la sonda
calibradora, mientras se mantiene la presión sobre la rama de Roux un poco más
allá de la anastomosis, debe lograrse una distensión sin fugas.(18)
Cierre de
defectos mesentéricos:
La
rama retrocólica de Roux debe fijarse a una estructura confiable para evitar
que proyecte detrás del estómago, prevenimos esto virando la rama de Roux a la
porción proximal adyacente de la rama biliopancreática, justo distal al
ligamento Treitz, con varias suturas no absorbibles, también se sutura la rama
de Roux con el defecto mesentérico tanto por encima como lateralmente al lado
izquierdo del paciente para prevenir la herniación en cualquiera de estas
áreas.(18)
El
bypass gástrico en Y de Roux (BGYR) produce una pérdida de peso substancial y
sostenida. Además, este tipo de tratamiento quirúrgico para la obesidad conduce
también a la mejoría en el estado de la mayoría pacientes con Diabetes Mellitus
tipo 2 (DM2). Reportándose en varias series de estudios, después del año de la
cirugía, un resultado eficaz para una reducción de peso significativo de
alrededor del 60% de pérdida del sobrepeso corporal y una resolución clínica y
bioquímica del 82% de la DM2 definida como normoglicemia sin medicación, con
el 18% restante logrando una mejoría significativa de su diabetes.(17)
La
remisión de la diabetes se produce en pocos días, incluso mucho antes de una
pérdida de peso significativa. Estas observaciones indican que los mecanismos a
través de los cuales el BGYR conduce a la mejoría del estado glucémico van más
allá que aquellos relacionados a la pérdida de ponderal, como podrían ser un
aumento a la sensibilidad hepática a la insulina o reducción en la producción
de glucosa endógena basal. Sumándose además una mejoría en la sensibilidad
hepática a la insulina sin cambios en la sensibilidad periférica, esta es la
respuesta típica a la restricción calórica en sujetos obesos independientemente
de la tolerancia a la glucosa, y se asocia con una disminución temprana de la
grasa hepática.(19)
BYPASS GÁSTRICO DE UNA SOLA ANASTOMOSIS
(BAGUA):
Es
el procedimiento simplificado del ¨tradicional¨ bypass gástrico en Y de Roux,
tras su aparición, la prevalencia de BAGUA en sus inicios fue mínima ya que
surgieron muchas controversias se sus posibles complicaciones, incluyendo el
reflujo alcalino crónico y sus consecuencias, lo que la hizo menos popular
inicialmente; sin embargo, el bypass gástrico de una sola anastomosis se ha ido
perfeccionando a lo largo del tiempo obteniendo múltiples ventajas, como la de
tener una anastomosis menos, un menor tiempo operatorio, menor riesgo de fuga
anastomótica y menos riesgo de hernia interna, además de poseer una curva de
aprendizaje más corta y la facilidad de reversibilidad, lo que lo hace cada vez
más utilizado.(20)
El
bypass gástrico de una sola anastomosis se propuso como un tratamiento simple y
efectivo para Obesidad Mórbida, y luego de varias décadas realizándose esta
técnica, se adoptó el concepto ¨mini bypass gástrico¨ (MBG) desarrollando
ajustes para contrarrestar sus principales críticas. Así es como varios autores
acuñaron el término de mini bypass gástrico de una sola anastomosis
(MBG-OAGB) o en español simplemente BAGUA, al referirse a este procedimiento
modificado.(21)
Figure 3
Representación Esquemática del bypass gástrico de una Sola Anastomosis (BAGUA)
Con bolsa gástrica de 18 a 20cm y una anastomosis laterolateral. El asa
aferente está suspendida 8 a10 cm por encima de la anastomosis. (efecto de
Válvula antireflujo)
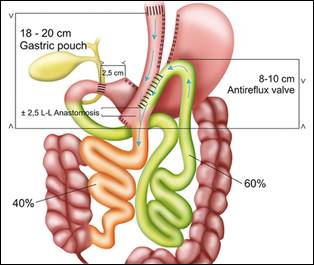
BAGUA consiste en la
construcción de una bolsa gástrica desde la unión gastroesofágica hasta el
nivel inferior de la cisura angularis. La línea de grapado de la bolsa gástrica
se fija aproximadamente 12 cm al asa intestinal (primera capa de mecanismo antirreflujo),
y se anastomosa en una posición laterolateral al borde mesentérico del asa
yeyunal a 200 cm (IMC 35 - 40), 250 cm (IMC 40-45) y 280 cm (IMC 45-50) distal
al ligamento Treitz, dicha distancia puede variar según el grado de obesidad.
Posteriormente se realiza la anastomosis sobre esta primera capa que crea una
barrera que separa ambas cavidades: estómago e intestino, evitando la entrada
de secreción biliopancreática al estómago y añadiendo restricción al estómago
vacío. El mecanismo antireflujo se completa fijando el asa aferente al
remanente gástrico y el asa eferente al antro.(22)
Técnica Quirúrgica:
Se
realiza típicamente de manera laparoscópica, usando 5 o 6 trócares
habitualmente. El primer paso consiste en localizar el ligamento de Treitz, y
posteriormente se mide el asa yeyunal que se desea desfuncionalizar, que en
los reportes iniciales de esta técnica eran de 200 cm, pero después de
publicarse varios resultados, se comenzó a medir todo el intestino delgado
rutinariamente desde el ángulo de Treitz hasta la válvula ileocecal, para
determinar la extensión de Intestino delgado anulado (asa aferente) y el canal
común alimentario (asa eferente); se selecciona la porción media y, por lo
tanto, sus longitudes son generalmente similares entre 250 a 350 cm. Para
aumentar la pérdida de peso de acuerdo al IMC del paciente, se agrega de 10 a
50 cm de intestino delgado anulado, pero siempre se mantiene al menos 250 a 300
cm de canal común. Por lo tanto, la extensión de intestino delgado omitido se
basa en la longitud total intestino delgado.(23)
El
paciente luego se coloca en una posición anti-Trendelenburg de 30 ° para
identificar el ángulo de His, y la almohadilla de grasa de la unión el
esófago-gástrica explícitamente se disecada para visualizar el pilar izquierdo
del diafragma obteniéndose un posicionamiento óptimo del endostapler en esta
ubicación crítica. En pacientes con hernia hiatal asociada, este paso incluye
la sección de adherencias periesofágicas y del ligamento frenoesofágico para
reducir la hernia, el cierre hiatal se realiza de forma selectiva.(23)
Posteriormente
se utiliza el bisturí ultrasónico para seccionar la grasa de la curvatura
gástrica menor y los vasos sanguíneos a nivel de la pata de cuervo para entrar
en el omento menor. Una grapadora endoscópica cargada con un cartucho de 45
mm/3,5 mm (Endo-GIA) es insertada a través de la apertura creada, seccionando
el estómago horizontalmente.(23)
Se
inserta una sonda orogástrica con doble luz de 36 French para calibrar el
depósito gástrico. El tejido graso y las adherencias fibrosas entre la pared
gástrica posterior y el páncreas son disecadas luego; se aplica
consecutivamente 3 disparos por lo general, con una grapadora endoscópica
cargada con cartuchos de 60 mm/3.5 mm, seccionando el estómago verticalmente y
completando el reservorio gástrico. Este último debe ser largo, estrecho, bien
vascularizado y fácil de mover caudalmente. Se extrae la sonda orogástrica y el
intestino delgado previamente elegido se moviliza hacia arriba colocándolo sin
tensión en una posición antecólica, antegástrica.(23)
Se
realiza una sutura contínua con material reabsorbible no. 2-0 en una posición
laterolateral, fijando el asa de intestino a la línea de grapado del reservorio
gástrico a lo largo de 8 a 10 cm. Posteriormente se realiza con ayuda del
bisturí ultrasónico una enterotomía y una gastrostomía a nivel del reservorio
gástrico distal, para luego insertar parcialmente (un 75%) una grapadora
endoscópica cargada con cartucho de 30 mm/3.5mm y es aplicada entre ambos,
creando así una anastomosis gastroentérica de 2 a 2.5 cm de largo.(23)
Las
Incisiones en la pared anastomótica anterior se suturan con material
reabsorbible No. 2-0 mediante puntos discontinuos. Estos también se utilizan
para sujetar el asa biliopancreática (asa aferente) en dirección ascendente de
8 a 10 cm hacia el estómago excluido, y también el asa común (eferente) al
antro gástrico excluido. Estas medidas descargan tensión de la anastomosis,
mejora su orientación y refuerza el mecanismo antirreflujo. La integridad de la
anastomosis se verifica con una prueba neumática, por último, se coloca un
drenaje de penrose debajo lóbulo hepático izquierdo y es sacado a través de la
incisión subcostal derecha de 5 mm.(23)
BAGUA
ha sido promovido como una alternativa técnicamente más fácil y segura al
bypass gástrico en Y de Roux (BGYR), ya que no requiere de una anastomosis
gastrointestinal adicional. Demostrando ser una técnica segura y efectiva,
reduciendo la dificultad quirúrgica, el tiempo de operación y las
complicaciones tempranas y tardías que se producen con e BGYR. Varias series de
estudios reportan que la pérdida de peso a largo plazo, la resolución de las
comorbilidades y el grado de satisfacción son similares a los resultados
obtenidos con técnicas más agresivas y complejas. Actualmente es una
alternativa robusta y poderosa en cirugía bariátrica.(21)
La evidencia publicada ha demostrado la
eficacia de la cirugía bariátrica en determinar la remisión de la diabetes
mellitus tipo 2 (DM2). La superioridad de la cirugía, incluso en comparación
con el tratamiento conservador ha llevado a muchos autores a investigar
diferentes mecanismos capaces de mejorar o curar la DM2 en pacientes con
obesidad. Cada vez existen más
pruebas indicando que el impacto del bypass gástrico sobre la DM2 no puede
explicarse únicamente por los efectos de la pérdida poderal y la reducción de
la ingesta energética, sumándose así otras acciones antidiabéticas
independientes del peso, siendo evidentes debido a la resolución muy rápida de
la DM2 incluso antes de que ocurra la pérdida de peso.(24)
La
cirugía metabólica atenúa el apetito, modifica las tendencias alimenticias,
promueve la homeostasis de la glicemia disminuyendo la resistencia hepática a
la insulina y mejora la secreción pancreática de la insulina. La remisión de la
DM2 es consecuencia del incremento de la sensibilidad a la insulina y el
mejoramiento de la función de las células beta pancreáticas.(24)
En
2009, Cummings revisó las conjeturas existentes sobre los mecanismos endócrinos
subyacentes de remisión de la diabetes posterior a la realización de cirugía de
bypass gástrico, basado en este estudio, tres principales hipótesis se
postularon: La hipótesis de la grelina, una hormona secretada por las células
del fundus gástrico que promueve la resistencia a la insulina, esta hipótesis
afirma una liberación afectada de esta hormona después de realizarse un bypass
gástrico. La disminución de la secreción de grelina puede, de hecho, disminuir
el apetito y la ingesta de alimentos en estos pacientes, también aumenta la
tolerancia a la glucosa, dado que la grelina puede estimular las hormonas
contrarreguladoras. (19)
La
hipótesis de exclusión del intestino superior establece, que al evitar el
contacto de nutrientes con el duodeno es de alguna manera una clave en el
proceso a través del cual se mejora el metabolismo de la glucosa, ya
que se ha reportado un aumento notable de la tolerancia a la glucosa posterior
a las intervenciones que involucran la exclusión duodenal, como es el caso del
bypass gástrico. Se presume que el contacto de los nutrientes con la mucosa
duodenal desencadena señales hormonales y neurales que repercuten en la
tolerancia a la glucosa y en la secreción de insulina.(19)
Finalmente,
la hipótesis del intestino inferior, como mecanismo de impacto antidiabético directo, afirma que los atajos
intestinales creados por el bypass gástrico, agiliza la entrega de los
nutrientes ingeridos y aumenta la liberación del péptido similar al glucagón -
1 (GLP-1) desde el intestino delgado
con una estimulación mejorada de estos péptidos en las células L, promoviendo
así la liberación de insulina dependiente de glucosa. Sus altos niveles luego
de realizar el bypass gástrico hacen pensar que participa en la mejoría de la
función de las células beta. (24)
Por
lo tanto, es interesante observar cómo a partir de varios metaanálisis, se
confirma que los procedimientos bariátricos sobre todo el bypass gástrico, son
capaces de proporcionar una aceptable y duradera remisión de la DM2 mediante la
intervención de al menos una de las tres hipótesis. (15)
Balance
energético y sensibilidad alterada a la insulina
El
incremento del tejido adiposo se ha relacionado evidentemente con el aumento de
la producción de citoquinas proinflamatorias, que, en conjunto a los ácidos
grasos, provocan el desarrollo de la resistencia a la insulina. La pérdida de
peso luego de la cirugía corresponde a una depleción de grasa tanto subcutánea
como visceral. Esta disminución de adiposidad logra una reversión del estado
inflamatorio crónico, e incrementa la secreción de adiponectina, mejorando la
sensibilidad a la insulina en el tejido adiposo.(25)
De
forma habitual la disminución de la adiposidad promueve claramente la
sensibilidad hepática y del músculo esquelético a la insulina. También existe
reversión de las alteraciones en el metabolismo de la glucosa y la lipólisis,
posiblemente por cambios en la actividad endócrina del tejido adiposo y por la
restricción calórica.(25)
Indicaciones del Bypass Gástrico en cirugía
metabólica:
Las indicaciones de
la cirugía metabólica han ido evolucionando a lo largo del tiempo, desde la
1era reunión del consenso americano del Panel de expertos del Instituto
Nacional de la Salud (NIH), al igual que otras sociedades científicas europeas,
que posteriormente añadieron varios criterios de inclusión los cuales indican:(26)(27)
·
Pacientes con un IMC igual o > 40 kg/m2.
·
Pacientes con un IMC igual o >35 kg/m2 con
comorbilidad relacionada grave. (Dislipidemia aterogénica, hipertensión, SAOS o
alteraciones
osteoarticulares significativas, que no responden a terapias médicas.)
·
Pacientes
con un IMC igual o > 35 kg/m2 con DM2.
·
De
acuerdo con las recomendaciones actuales, los pacientes con obesidad clase I
(IMC >30 kg/m2) con DM2 mal controlada y riesgo cardiovascular aumentado
tras una valoración individualizada de un comité multidisciplinar.(28)
RESULTADOS
Se analizaron 76 pacientes para
comparar la eficacia del bypass gástrico laparoscópico de una sola anastomosis
(BAGUA) frente al bypass gástrico en ¨Y de Roux¨ (BGYR), los cuales tenían
diagnóstico de Obesidad y diabetes mellitus tipo 2, operados en el Hospital
“Abel Gilbert Pontón”, durante el periodo de enero 2015 a diciembre 2019.
Figure 4 Distribuciones y frecuencias
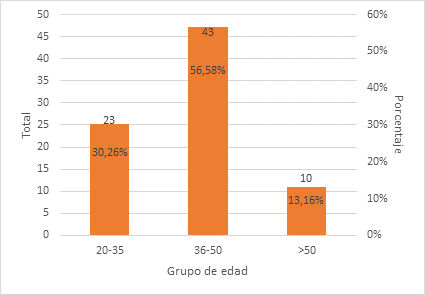
Fuente: Elaboración
propia a través de los archivos del Hospital Abel Gilbert Pontón
Análisis e
Interpretación:
dentro
de los pacientes sometidos a bypass gástrico, la media de edad fue de 40 años.
Por grupo etario se observó una mayor proporción de pacientes representando el
56,58% entre los 36 a 50 años, seguido de 30,26% entre los 20 a 35 años, y
13,16% >50 años.
Figure 5
Distribución de los pacientes según el sexo
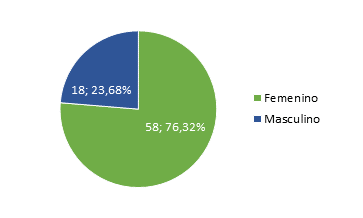
Fuente: Elaboración
propia a través de los archivos del Hospital Abel Gilbert Pontón.
Análisis
e Interpretación: dentro de los 76 pacientes sometidos a
bypass gástrico analizados, se observó predominio del sexo femenino 76,32%,
mientras del masculino 23,68%.
Figure
6
Clasificación de los tipos de obesidad en personas que se realizaron el bypass.
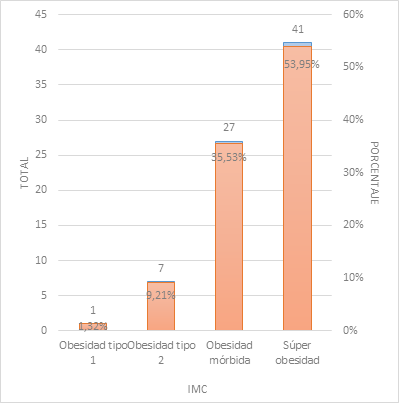
Fuente: Elaboración
propia a través de los archivos del Hospital Abel Gilbert Pontón.
Análisis
e Interpretación: dentro de los pacientes sometidos a bypass
gástrico analizados, la media del IMC Preoperatorio fue de 52 kg/m2,
de acuerdo a la clasificación de Obesidad, se observó 53,95% de pacientes con
súper obesidad, 35,53% obesidad mórbida, 9,21% obesidad tipo 2 y 1,32% obesidad
tipo 1.
Análisis
e Interpretación: dentro de los pacientes sometidos a
bypass gástrico analizados, la media de la Glicemia Prequirúrgica se ubicó en
130,55 mg/dl; al clasificar los valores de glicemia se observó 27,63% con
valores normales (<100 mg/dl), 27,63% en rango de prediabetes (100 a 126
mg/dl), 21,05% con hiperglicemia leve (127 a 140 mg/dl), 17,11% hiperglicemia
moderada (141 a 250 mg/dl) y 6,58% hiperglicemia severa (>250 mg/dl).
Figure 7
Distribución de los pacientes según niveles de Glicemia Prequirúrgica.
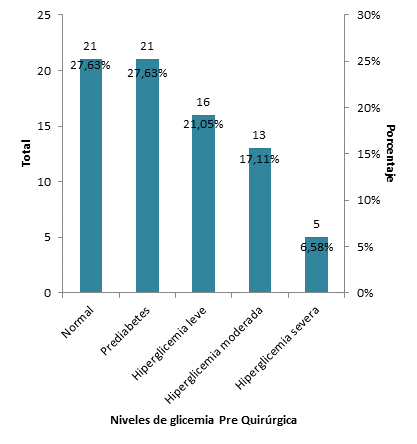
Fuente: Elaboración
propia a través de los archivos del Hospital Abel Gilbert Pontón.
Análisis
e Interpretación: dentro de los 76 pacientes sometidos a
bypass gástrico analizados, 60,53% se realizó bypass gástrico laparoscópico
mediante BAGUA y 39,47% mediante Y de Roux (BGYR).
Figure
8 Distribución
de los pacientes según técnica quirúrgica utilizada
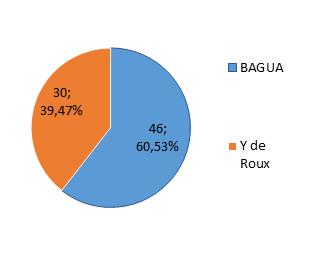
Fuente:
Elaboración propia a través de los archivos del Hospital Abel Gilbert Pontón.
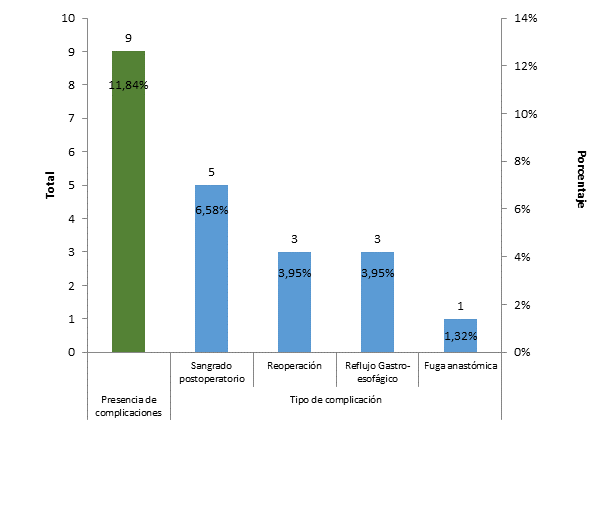
Análisis
e Interpretación: dentro de los pacientes sometidos a
bypass gástrico, El 11,84% de los pacientes presentaron algún tipo de
complicaciones, siendo la más frecuente el sangrado postoperatorio con 6,58%,
seguido de reoperación 3,95% e igual porcentaje para reflujo gastro-esofágico y
1,32% fuga anastomótica.
Figure
9 Distribución
de los pacientes según complicación
Fuente: Elaboración
propia a través de los archivos del Hospital Abel Gilbert Pontón.
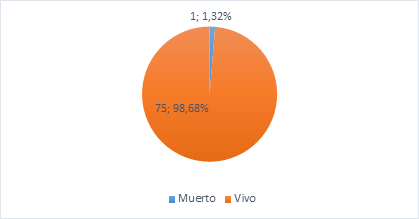
Análisis
e Interpretación: Solo falleció un paciente de los 76
analizados, lo que representa 1,32%, el paciente fallecido había sido
intervenido mediante técnica de ¨Y de Roux¨.
Figure
10 Distribución
de los pacientes según condición de egreso
Fuente: Elaboración
propia a través de los archivos del Hospital Abel Gilbert Pontón.
CONCLUSIONES
v
En
cuanto a las características de los pacientes sometidos a bypass gástrico,
tenemos que la edad promedio se ubicó en 45 años; fueron 76,32% mujeres y 23,68%
hombres; el IMC Preoperatorio promedio fue de 52 kg/m2; de acuerdo a la
clasificación de Obesidad, se observó un 53,95% de pacientes que tenían
Superobesidad, 35,53% Obesidad Mórbida, 9,21% obesidad tipo 2 y 1,32% obesidad
tipo 1 al momento de la cirugía; el nivel de glicemia prequirúrgica promedio se
ubicó en 130,55 mg/dl; el 27,63% de pacientes presentó valores normales de
glicemia, 27,63% en rango de prediabetes, 21,05% con hiperglicemia leve,
17,11% hiperglicemia moderada y 6,58% hiperglicemia severa; el control de Hb
A1C preoperatoria tuvo una media del 6,08%, donde el 72.37% de los pacientes
presentaron un control preoperatorio ideal con valores de Hb A1C <6,5%;
13.16% de los pacientes tuvieron entre 6,5 a 7% catalogados como control aceptable
y 14,47% presentaron valores >7%, correspondientes a un mal control
preoperatorio; de acuerdo a la técnica quirúrgica elegida, el 60,53% se
realizaron bypass gástrico laparoscópico mediante BAGUA y 39,47% mediante Y de
Roux (BGYR).
v
Al
comparar el Porcentaje de Sobrepeso Perdido (PSP), la Pérdida Total de Peso
(PTP) y el Porcentaje de Exceso de IMC Perdido (PEIMCP) entre las 2 técnicas
quirúrgicas, no mostraron diferencias significativas en ninguno de los tiempos
de seguimiento (3, 6 y 12 meses), sin embargo, se obtuvo mayores porcentajes de
pérdida de peso en BAGUA.
v
Según
los indicadores de eficacia en respuesta a la pérdida de peso 12 meses
posterior a cirugía, se observó mayor proporción de los pacientes sometidos a
BAGUA con una excelente respuesta a la pérdida de peso (PSP y PEIMCP >65%),
en comparación a una proporción menor en los pacientes con BGYR.
v
Al
comparar los niveles de glicemia y de Hb A1C a los 3 y 6 meses postquirúrgicos,
no hubo diferencia significativa entre las 2 técnicas, no obstante, a los 12
meses presentaron diferencia significativa (p-valor 0,049) para glicemia las
medias fueron 88,76 mg/dl en BAGUA vs 93,38 mg/dl en BGYR; y para Hb A1C a los
12 meses las medias fueron de 4,85% para BAGUA vs 5,12% para BGYR (p-valor 0,010).
v
Basado
en los resultados, este estudio sugiere que BAGUA es un procedimiento eficaz
para la pérdida de peso en pacientes con obesidad, con iguales o mejores
beneficios que el BGYR, y posee mayor efectividad en remisión completa de
diabetes mellitus en comparación con BGYR (p-valor 0,023);
además, parece ser más seguro con menor morbilidad y menos porcentaje de
reoperación (p-valor 0,029). Su sencillez en la técnica representa una ventaja
real, se reduce la dificultad quirúrgica, el tiempo de operación
(p-valor ≈ 0,000), estancia hospitalaria (p-valor 0,013), y
complicaciones tempranas que se presentan con el bypass gástrico en Y de Roux,
evidenciando excelentes resultados de pérdida de peso, control metabólico y
menor uso de hipoglicemiantes (p-valor 0,013),
lo que lo convierte en una opción que debe ser considerada por todos los
cirujanos. Sin embargo, la desnutrición proteica, anemia y el reflujo biliar
son posibles inconvenientes del BAGUA.
v
El
BGYR, es técnicamente exigente, necesita de una anastomosis más, siendo un
procedimiento con una morbilidad relativamente mayor y necesidad aumentada de
ingresos a sala de UCI (p-valor 0,021).
Se presentó fuga anastomótica y sangrado postoperatorio (p-valor 0,055) en
mayor proporción de pacientes sometidos a BGYR; mientras que, en BAGUA se
observó mayor porcentaje de reflujo gastroesofágico, hipoalbuminemia
leve/moderada y anemia leve (p-valor 0,001).
v
Falleció
un paciente de los 76 analizados, lo que representa 1,32%, el paciente
fallecido había sido intervenido mediante Y de Roux, mientras que se presentó
0% de mortalidad en los pacientes sometidos a BAGUA.
BIBIOGRAFÍA
1.
Organización
Mundial de la Salud. Obesidad y Diabetes [Internet]. 2016. Available from: www.paho.org/es/temas/diabetes
2.
Hermosillo-Cornejo DG, Arreola-Ramírez DA, Girón-Gidi AD,
Álvarez-hernández DA, López-caballero C. Cirugía bariátrica y metabólica , una
perspectiva histórica desde sus inicios. MEDIGRAPHIC
- EL Resid. 2016;11(2):88–95.
3. Ramos A, Kow L, Brown W, Welbourn R, Dixon J,
Kinsman R, et al. The IFSO Global Registry: 5th IFSO Global Registry Report
2019 [Internet]. United Kingdom; 2019. 6–8 p. Available from: https://www.ifso.com/pdf/5th-ifso-global-registry-report-september-2019.pdf
4.
Sociedad Americana de Cirugía Bariatrica y Metabólica. Cirugía para la
diabetes [Internet]. 2020. Available from: https://asmbs.org/patients/surgery-for-diabetes
5. Mahawar K. Bariatric Surgery : The Past
, the Present , and the Future Bariatric Surgery : The Past , the Present
, and the Future. Webmedcentral. 2012;3:1–7.
6. Scopinaro N. Thirty-Five Years of
Biliopancreatic Diversion : Notes on Gastrointestinal Physiology to
Complete the Published Information Useful for a Better Understanding and
Clinical Use of the Operation. OBES SURG. 2012;22:427–32.
7. Rutledge R, Kular K, Manchanda N. The
Mini-Gastric Bypass original technique. Int J Surg [Internet]. 2019;61:38–41.
Available from: https://doi.org/10.1016/j.ijsu.2018.10.042
8.
De Luca M, Tie T, Ooi G, Higa K, Himpens J, Carbajo M, et al. Mini
Gastric Bypass-One Anastomosis Gastric Bypass (MGB-OAGB)-IFSO Position
Statement. Obes Surg. 2018;28(5):1188–206.
9. Cohen R, Le Roux C, Junqueira S, Ribeiro R,
Luque A. Roux-En-Y Gastric Bypass in Type 2 Diabetes Patients with Mild
Obesity: a Systematic Review and Meta-analysis. Obes Surg.
2017;27(10):2733–9.
10.
Organización Mundial de la Salud. Informe mundial sobre la diabetes: 8 de
junio de 2020 [Internet]. 2020. Available from: www.who.int/es/news-room/fact-sheets/detail/diabetes
11. Rowley WR, Bezold C, Arikan Y. Diabetes 2030:
Insights from Yesterday, Today, and Future Trends. Popul
Health Manag. 2016;20:1–7.
12.
Instituto Nacional de Estadística y Censos (INEC). Registro Estadístico de
Defunciones Generales. Informe 2019. [Internet]. 2019. Available from: www.ecuadorencifras.gob.ec/documentos/web-inec/Poblacion_y_
Demografia/Nacimientos_Defunciones/2020/Boletin_ tecnico_ EDG 2019 prov.pdfle
13.
Organización Panamericana de la Salud. La diabetes, un problema
prioritario de salud pública en el Ecuador y la región de las Américas.
Encuesta Nacional de Salud y Nutrición (ENSANUT) [Internet]. 2018. Available
from: www.paho.org/ecu/index.php?option=com_content&
view=article&id=1400:la-diabetes-un-problema-prioritario-de-salud-publica-en-el-ecuador-y-la-region-de-las
americas&Itemid=360#:~:text= En Ecuador%2C diabetes están afectando,diez
ecuatorianos ya tiene diabetes
14.
Organización Mundial de la Salud. Obesidad y Sobrepeso [Internet]. 2020. Available
from: www.who.int/es/news-room/fact-sheets/detail/obesity-and-overweight
15. Buchwald H, Estok R, Fahrbach K, Banel D, Jensen
MD, Pories WJ, et al. Weight and Type 2 Diabetes after Bariatric Surgery:
Systematic Review and Meta-analysis. Am J Med [Internet]. 2009;122(3):248–56.
Available from: http://dx.doi.org/10.1016/j.amjmed.2008.09.041
16. Magouliotis DE, Tasiopoulou VS, Tzovaras G. One
Anastomosis Gastric Bypass Versus Roux-en-Y Gastric Bypass for Morbid Obesity:
an Updated Meta-Analysis. Obes Surg. 2019;29(9):2721–30.
17. Schauer PR, Burguera B, Ikramuddin S, Cottam D,
Gourash W, Hamad G, et al. Effect of Laparoscopic Roux-en-Y Gastric Bypass on
Type 2 Diabetes Mellitus. Univ Otago Libr. 2014;60–1.
18.
Schirmer B, Hallowell P. Obesidad Mórbida y su tratamiento quirúrgico;
Bypass Gástrico en Y de Roux Laparoscópico. In:
Zinner MJ, Ashley SW, editors. Cirugías Abdominales de Maingot. 12va ed. 2018.
p. 558–64.
19. Cummings DE. Endocrine mechanisms mediating
remission of diabetes after gastric bypass surgery. Int J Obes [Internet].
2009;33(S1):33–40. Available from: http://dx.doi.org/10.1038/ijo.2009.15
20. Quan Y, Huang A, Ye M, Xu M, Zhuang B, Zhang P,
et al. Efficacy of Laparoscopic Mini Gastric Bypass for Obesity and Type 2
Diabetes Mellitus: A Systematic Review and Meta-Analysis. Gastroenterol Res
Pract. 2015;2015.
21. Parikh M, Eisenberg D, Johnson J, El-chaar M,
Kothari SN. American Society for Metabolic and Bariatric Surgery Review of the
Literature on One-Anastomosis Gastric Bypass Manish. Surg Obes Relat Dis
[Internet]. 2018;14:502–21. Available from: https://doi.org/10.1016/j.soard.2018.04.017
22. Garcia caballero M, Reyes Ortíz A, García M,
Matínez Moreno A. Changes of Body Composition in Patients with BMI 23 – 50
After Tailored One Anastomosis Gastric Bypass ( BAGUA ): Influence of Diabetes
and Metabolic Syndrome. 2014;2040–7.
23.
Carbajo MA, Luque-de-León E, Jiménez JM, Ortiz-de-Solórzano J, Pérez-Miranda
M, Castro-Alija MJ. Laparoscopic One-Anastomosis Gastric
Bypass: Technique, Results, and Long-Term Follow-Up in 1200 Patients. Obes Surg
[Internet]. 2017;27(5):1153–67. Available from: http://dx.doi.org/10.1007/s11695-016-2428-1
24.
Musella M, Apers J, Rheinwalt K, Ribeiro R, Manno E, Greco F, et al. Efficacy
of Bariatric Surgery in Type 2 Diabetes Mellitus Remission: the Role of Mini
Gastric Bypass/One Anastomosis Gastric Bypass and Sleeve Gastrectomy at
1 Year of Follow-up. A European survey. Obes Surg.
2016;26(5):933–40.
25.
Ros Pérez M, Medina Gómez G. Obesidad , adipogénesis y resistencia a la
insulina. Endocrinol Y Nutr. 2011;58(7):360–9.
26.
Pacheco Sánchez D, Pinto Fuentes P, Enrique Asensio D. Actualización en
cirugía bariátrica / metabólica. Nutr Clínica en Med [Internet].
2019;XIII:113–27. Available from: https://www.ifso.com/pdf/5th-ifso-global-registry-report-september-2019.pdf
27.
Fried M, Yumuk V, Oppert JM, Scopinaro N,
Torres A, Weiner R, et al. Interdisciplinary European Guidelines on Metabolic
and Bariatric Surgery. Obes Surg. 2014;24:42–55.
28.
Díez I, Martínez C, Ruiz J, De La Cruz F, Torres A. Recomendaciones de la
SECO para la práctica de la cirugía bariátrica y metabólica ( Declaración de
Vitoria-Gasteiz , 2015 ). Bariatrica Metabólica Iberoam. 2015;3:842–5.
29.
García García M, Martím Lorenzo J, Lirón Ruiz R, Torralba Martínez J.
COMPLICACIONES POSTOPERATORIAS TRAS CIRUGÍA BARIÁTRICA. CLASIFICACIÓN Y
VALIDACIÓN SEGÚN CLAVIEN-DINDO. EXPERIENCIA EN NUESTRO CENTRO Y REVISIÓN DE LA
LITERATURA. Cirugía Española. 2019;97:2–8.